Uma via terciária para a oxidação do etanol é realizada por catalase, uma enzima peroxisomal que também catalisa a remoção do peróxido de hidrogénio (H2O2). Embora a catalase tenha um papel muito menor na oxidação do álcool do que o ADH ou CYP2E1, é importante na função cerebral, pois verificou-se que a catalase inibidora diminui a taxa de oxidação do etanol em acetaldeído pelo cérebro (3).
Em condições com alta concentração de peróxido de hidrogénio, a catalase trabalha para converter duas moléculas de H2O2 em duas moléculas de água. A primeira molécula de H2O2 entra no local activo onde oxida o ferro de hémen para produzir um grupo oxyferryl com um radical de porfirina catiónico π e uma molécula de água. Uma segunda molécula de peróxido de hidrogénio entra então no local activo e é oxidada em oxigénio molecular e água. Em baixas concentrações de H2O2, contudo, uma via alternativa irá ocorrer devido à forte natureza oxidante do grupo oxidante formado após a oxidação da primeira molécula de H2O2. Os radicais hidroxil sairão do canal para o local activo e oxidarão moléculas de etanol para moléculas de acetaldeído fora do local activo (10).
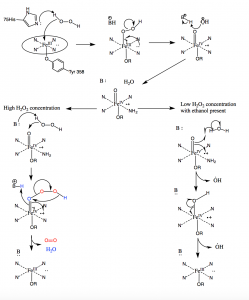
Figure 10: Mecanismo da catalase. Em condições de alto peróxido de hidrogénio, a catalase segue o mecanismo da esquerda para oxidar duas moléculas de peróxido. Sob baixas concentrações de peróxido de hidrogénio, a catalase segue o mecanismo dos radicais à direita e produz dois radicais hidroxil.
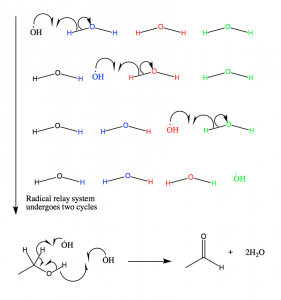
Figure 11: Os radicais hidroxil produzidos no mecanismo dos radicais catalase são canalizados para fora do local activo através deste mecanismo. Os radicais reagem então com etanol, que é mantido na proximidade do sítio activo. Se o etanol não estiver presente, o NADPH é oxidado.
O sítio activo da catalisase é uma hemorragia com a His-75 a desempenhar um papel importante na actividade catalítica; utiliza um relé de carga (resíduos Tyr358, Arg354, His218 e Asp348) a fim de realizar reacções sem perturbar a ligação do peróxido. Quando o grupo oxyferryl é formado, o sistema de relé de carga é iniciado através do movimento contínuo dos electrões de ligação de coordenação de uma ligação para a outra. A ressonância atribuída ao movimento dos electrões de ligação de coordenação permite a formação de uma nuvem de electrões em torno do centro de ferro, na qual os electrões podem ser doados às reacções catalíticas (10).
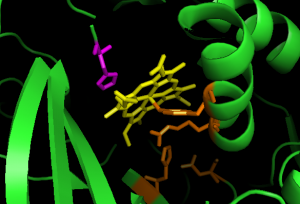
Figure 12: O local activo da catalase contém um heme (amarelo) com catalisador His75 no lado distal (roxo), e vários resíduos, Tyr358, Arg354, His218 e Asp348, contribuindo para um sistema de relé de carga no lado proximal, mostrado em laranja (ficheiro pdb: 1qqw).
0 comentários