La disponibilité et l’utilisation de l’avortement médicamenteux
L’avortement médicamenteux, également connu sous le nom d’avortement médical ou d’avortement par pilules, est un protocole d’interruption de grossesse qui implique la prise de deux médicaments différents, la mifépristone et le misoprostol, qui peuvent être utilisés en toute sécurité jusqu’aux 70 premiers jours (10 semaines) de la grossesse. Depuis que la Food and Drug Administration (FDA) a approuvé le médicament en 2000, son utilisation aux États-Unis s’est rapidement développée, plus d’un tiers des avortements à 8 semaines de gestation ou moins étant des avortements médicamenteux. Bien que ce protocole implique la prise de deux médicaments et n’implique pas de procédure médicale, il est soumis à bon nombre des mêmes restrictions spécifiques aux prestataires de services d’avortement que les autres méthodes d’avortement, tant au niveau des États qu’au niveau fédéral. Cette fiche d’information donne un aperçu de l’avortement médicamenteux, en mettant l’accent sur les réglementations fédérales et étatiques relatives à sa fourniture et à sa couverture, ainsi que sur le rôle du médicament dans les avortements autogérés.
Qu’est-ce qu’un avortement médicamenteux ?
Le régime d’avortement médicamenteux le plus courant aux États-Unis implique l’utilisation de deux médicaments différents : la mifépristone et le misoprostol. La mifépristone, vendue sous le nom de marque Mifeprex et également connue sous le nom de pilule abortive, RU-486, bloque la progestérone, une hormone essentielle au développement d’une grossesse, et empêche ainsi une grossesse existante de progresser. Le misoprostol, pris 24 à 48 heures après la mifépristone, agit pour vider l’utérus en provoquant des crampes et des saignements, semblables à ceux d’une fausse couche précoce. Une visite de suivi est généralement prévue une ou deux semaines plus tard, pour confirmer que la grossesse a été interrompue par une échographie ou un test sanguin. L’avortement médicamenteux est une méthode sûre et très efficace d’interruption de grossesse si les pilules sont administrées à 9 semaines de gestation ou moins, la grossesse est interrompue avec succès dans 99,6 % des cas, avec un risque de complications majeures de 0,4 % et un taux de mortalité associé inférieur à 0,001 % (0,00064 %).
Protocole de la FDA
Jusqu’en 2019, la mifépristone était uniquement vendue sous le nom de marque Mifeprex, fabriqué par Danco Laboratories. La FDA a approuvé le Mifeprex pour la première fois en 2000, et en 2016, elle a approuvé un nouveau régime fondé sur des données probantes et une nouvelle étiquette de médicament, qui guide la pratique clinique actuelle. Ce régime approuve l’utilisation des avortements médicamenteux jusqu’à 70 jours (10 semaines) de grossesse (tableau 1).
| Tableau 1 : Régime de la mifépristone et du misoprostol de la FDA | |
| Max. âge gestationnel | Jusqu’à 70 jours LMP* (10 semaines) |
| Dosage de la mifépristone | 200mg (un comprimé), pris par voie orale | Administration de la mifépristone | Dispensée en cabinet ; Le lieu où le médicament doit être pris (domicile ou milieu clinique) n’est pas précisé |
| 800µg (4 pilules), pris par voie buccale (placé dans la joue) ou vaginale | Misoprostol timing | 24-48 heures après la mifepristone par voie buccale, ou 6-72 heures après la mifépristone par voie vaginale | Prise à domicile | Visite de suivi | 7-14 jours après la mifépristone, aucun lieu spécifié |
| Exigences du prescripteur | Par ou sous la supervision d’un prescripteur qui a été certifié par le fabricant |
| Note : *LMP – Dernière période menstruelle | |
| Source : FDA, informations sur le mifeprex (mifépristone), février 2018. | |
Stratégies d’évaluation et d’atténuation des risques (REMS)
La mifépristone ne peut pas être délivrée par les pharmacies de détail comme la plupart des autres médicaments ; les patientes enceintes ne peuvent obtenir le médicament que directement auprès d’un prestataire médical certifié qui a rempli un formulaire d’accord de prescription du fabricant sur l’utilisation appropriée du médicament. Cela est dû au fait que la FDA applique une stratégie d’évaluation et d’atténuation des risques (REMS) pour le Mifeprex depuis 2011 (voir encadré 1).
Boîte 1 : Que sont les REMS et l’ETASU?
Depuis 2007, la FDA a le pouvoir d’exiger des fabricants de médicaments des programmes de stratégie d’évaluation et d’atténuation des risques (REMS) pour des médicaments spécifiques afin de s’assurer que ses avantages l’emportent sur ses risques. La FDA doit tenir compte de divers facteurs pour déterminer la nécessité d’un REMS, notamment : la gravité de la maladie ou de l’affection à traiter, la taille de la population susceptible d’utiliser le médicament, la durée prévue du traitement et la gravité des effets indésirables. Il existe actuellement 61 programmes REMS approuvés par la FDA. Ils sont généralement exigés pour les médicaments connus pour être associés à des complications graves potentielles ou à des contre-indications, comme les antipsychotiques, les opioïdes, la testostérone et les médicaments utilisés pour traiter le cancer, l’acné et la sclérose en plaques. Ces programmes peuvent inclure un guide du médicament, une notice pour le patient et/ou un plan de communication pour éduquer les prestataires sur l’utilisation sûre du médicament.
Si la FDA décide que ces mesures ne sont pas suffisantes pour autoriser en toute sécurité le médicament sur le marché, l’agence peut exiger une version plus stricte du REMS, comprenant un ou plusieurs éléments pour assurer une utilisation sûre (ETASU). Plus de la moitié des programmes REMS actuellement approuvés comportent un ou plusieurs ETASU. Les directives de la FDA stipulent qu’un ETASU « doit être proportionné au risque grave spécifique énuméré dans l’étiquetage du médicament, et ne doit pas être indûment contraignant pour l’accès au médicament, en particulier pour les patients atteints de maladies graves ou potentiellement mortelles et qui ont des difficultés à accéder aux soins de santé. »
Une variété d’organisations, telles que l’American College of Obstetricians and Gynecologists (ACOG), soutient l’élimination des règlements REMS pour la mifepristone, qui, selon elles, sont médicalement inutiles et entravent l’accès à l’avortement médical. L’ancienne commissaire de la FDA, Jane Henney, et le médecin Helene D Gayle ont publié un point de vue selon lequel la FDA devrait réévaluer les règlements REMS, à la lumière des études qui montrent que la mifepristone est sûre et efficace. Certains défenseurs suggèrent que le processus REMS limite le nombre de prestataires et, par conséquent, retarde les soins pour les patientes enceintes, car elles doivent rechercher des prestataires certifiés. Enfin, certains prestataires contestent devant les tribunaux la désignation REMS de la mifépristone.
Les directives et l’étiquette de la FDA pour le Mifeprex s’appliquent également au générique approuvé. Le programme REMS approuvé par la FDA pour le Mifeprex, et maintenant, la mifépristone générique, comprend également l’Element to Assure Safe Use (ETASU), une version plus forte du REMS, et contient trois dispositions :
- La mifépristone doit être délivrée aux patients uniquement dans certains établissements de santé, plus précisément les cliniques, les cabinets médicaux et les hôpitaux, par ou sous la supervision d’un prescripteur certifié ;
- Un prestataire doit devenir un prescripteur certifié en remplissant et en envoyant un formulaire d’accord du prescripteur au distributeur spécifique, Danco Laboratories ou GenBioPro, qui confirme qu’il est capable d’évaluer la durée d’une grossesse, de diagnostiquer les grossesses extra-utérines et de fournir un avortement chirurgical dans le cas d’un avortement incomplet;
- Le prescripteur certifié doit obtenir un formulaire d’accord du patient signé par la femme avant de délivrer le médicament, comme documentation des conditions d’utilisation sûre.1
Le 3 octobre 2017, l’American Civil Liberties Union (ACLU) a intenté un procès, au nom d’un groupe de prestataires, contre la FDA, contestant les exigences du REMS pour la mifepristone. Ces plaignants citent le faible taux de complications associées aux avortements médicamenteux et affirment que d’autres médicaments présentant des risques similaires ou plus graves ne sont pas soumis à des restrictions REMS, et sont indûment contraignants pour les patients qui tentent d’accéder au médicament, en particulier les patients des zones rurales ou médicalement défavorisées. Le tribunal de district d’Hawaï attend pour prendre des mesures dans cette affaire que la Cour suprême rende une décision dans l’affaire June Medical Services LLC v. Russo, qui concerne à la fois la « qualité de tiers » des prestataires pour engager des poursuites au nom de leurs patients, et l’évaluation de la « charge indue » dans les affaires d’avortement. En mai 2020, l’ACLU a déposé un autre procès contestant l’exigence REMS selon laquelle la mifepristone doit être délivrée en personne ; ce procès a été déposé au nom de l’American College of Obstetricians and Gynecologists (ACOG), en plus d’autres organisations.
Disponibilité
Les réglementations fédérales et au niveau des États ont effectivement limité l’utilisation de la mifepristone, en particulier dans les zones mal desservies sans clinique à proximité. Des études montrent que les prestataires d’avortement médicamenteux sont surtout concentrés là où l’avortement chirurgical est déjà disponible. De nombreuses lois étatiques réglementant les prestataires d’avortement s’appliquent à tous les types de procédures d’avortement. Par exemple, 17 États exigent que la clinique réponde à des normes structurelles comparables à celles des centres de chirurgie ambulatoire, comme le maintien de salles d’opération standard, de tables d’examen chirurgical, etc. Sept États exigent que les prestataires de services d’avortement disposent de privilèges d’admission à l’hôpital ou d’un autre arrangement en place. De nombreux États ont également adopté des lois concernant spécifiquement l’avortement médicamenteux, telles que des exigences spécifiques en matière de conseils et de prestataires. Actuellement, les 33 États n’autorisent que les médecins agréés à délivrer des pilules de mifépristone (figure 1). La recherche démontre que les cliniciens de pratique avancée (CPA), tels que les infirmières praticiennes, les assistants médicaux ou les infirmières sages-femmes, peuvent délivrer des pilules abortives de manière aussi sûre que les médecins, mais ils ne sont autorisés à le faire que dans 17 États et DC.
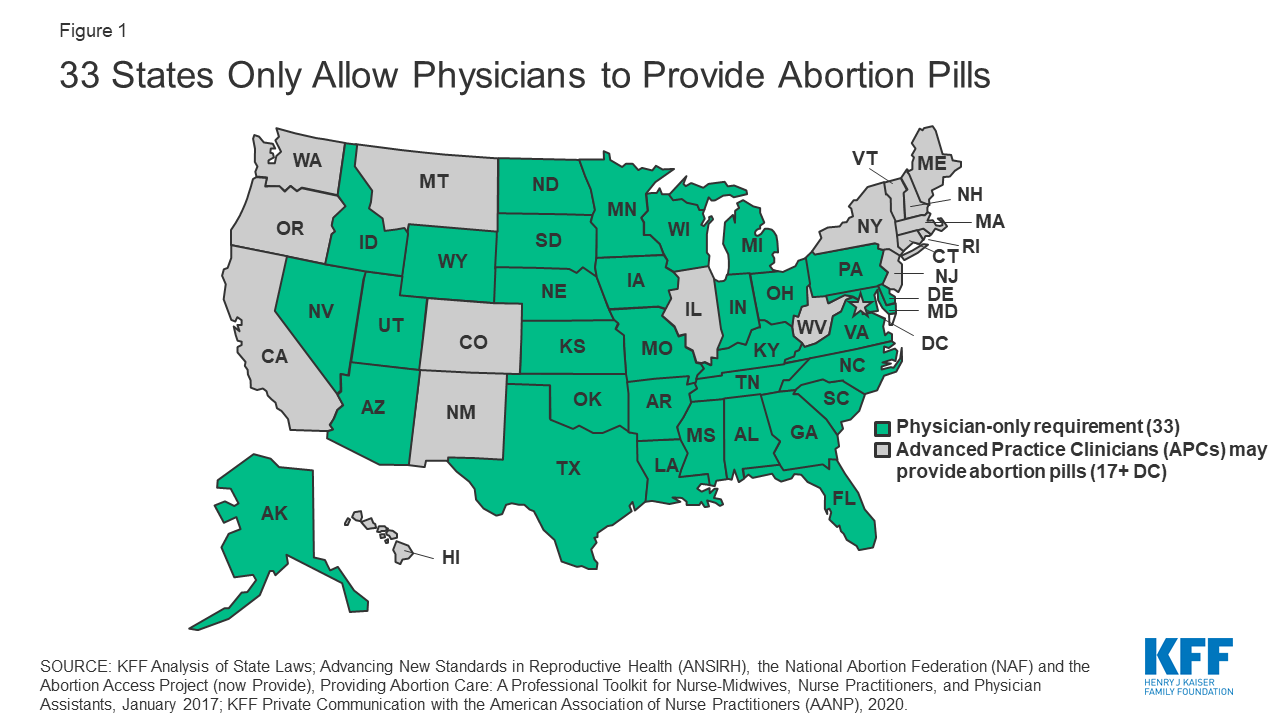
Figure 1 : 33 États n’autorisent que les médecins à fournir des pilules abortives
L’Arkansas, l’Idaho, le Kentucky, le Nebraska, l’Oklahoma, le Dakota du Sud et l’Utah ont adopté des lois qui obligent les prestataires à conseiller aux patientes que l’avortement médicamenteux peut être inversé si elles reçoivent une forte dose de progestérone après avoir pris de la mifépristone, malgré l’absence de preuves scientifiques à l’appui de cette affirmation. Des lois similaires ont été adoptées en Arizona, au Dakota du Nord et au Kansas, les tribunaux bloquant les lois en Arizona et au Dakota du Nord, et le gouverneur opposant son veto au projet de loi au Kansas.
Couverture d’assurance et coûts
La couverture d’assurance pour l’avortement est fortement réglementée au niveau fédéral et au niveau des États. Depuis 1977, l’amendement fédéral Hyde interdit l’utilisation de tout fonds fédéral pour l’avortement, sauf si la grossesse résulte d’un viol, d’un inceste ou s’il est déterminé que la vie de la femme est en danger. Après que la FDA a approuvé le Mifeprex en 2000, cette loi s’est également appliquée aux avortements médicamenteux. Cependant, une étude de 2019 du Government Accountability Office (GAO) américain a révélé que 14 programmes Medicaid d’État ne couvrent pas la mifépristone, même dans les cas de viol, d’inceste et de mise en danger de la vie, comme l’exige l’amendement Hyde.
Les États réglementent également les assurances privées entièrement assurées, y compris les plans sur les marchés de l’Affordable Care Act (ACA). 11 États limitent la couverture de l’avortement dans les plans d’assurance privée – certains de ces États suivent les exceptions de Hyde, tandis que d’autres sont plus restrictifs. En 2020, 33 États n’avaient aucun plan du marché de l’ACA offrant une couverture de l’avortement, 26 États l’interdisant catégoriquement. Plusieurs plans qui offraient une couverture pour les procédures d’avortement ne couvraient pas l’avortement médicamenteux, et certains plans qui offraient une couverture pour l’avortement présentaient des différences dans les limites de gestation, les plafonds annuels/à vie des demandes de remboursement et la couverture de la mifépristone. A l’inverse, six Etats (Californie, Illinois, Maine, New York, Oregon et Washington) exigent que tous les plans de santé privés réglementés par l’Etat (y compris les plans du Marché) incluent la couverture de l’avortement. Les régimes auto-assurés ne sont pas réglementés par la loi sur les assurances de l’État, et la loi fédérale n’interdit ni n’exige la couverture de l’avortement dans les régimes auto-assurés. Bien qu’il n’y ait pas eu de recherche récente sur la couverture de l’avortement offerte par les plans entièrement assurés dans les 33 États restants et le district de Columbia, Danco Laboratories propose un recueil des politiques des payeurs de l’État et de la façon dont elles se rapportent à Mifeprex.
En 2014, le montant moyen payé pour un avortement médicamenteux jusqu’à 10 semaines était de 535 $, tandis que le montant moyen payé pour un avortement dans une clinique et une anesthésie locale était de 508 $. Bien que Danco Laboratories ne rende pas public le coût du Mifeprex, les prestataires indiquent que le Mifeprex leur coûte environ 90 dollars par pilule. GenBioPro, le fabricant du médicament générique mifepristone ne rend pas non plus public le coût de sa pilule, mais a déclaré vouloir faire baisser les coûts pour ceux qui choisissent l’avortement médicamenteux.
Pour ceux qui n’ont pas de couverture pour l’avortement, il existe d’autres moyens limités de soutien financier, promus sur le site de Danco et de GenBioPro. La Fédération nationale de l’avortement, ainsi que les fonds locaux pour l’avortement sont parfois en mesure de couvrir une partie du coût d’un avortement (y compris le voyage) pour une personne enceinte. En dehors de ces sources de financement ou d’une clinique à tarif dégressif, il existe peu d’options pour aider à payer les coûts de l’avortement.
Utilisation
Bien que le taux global d’avortement ait continué à baisser, l’utilisation de l’avortement médicamenteux a considérablement augmenté au fil des ans, et représente maintenant environ 41% de tous les avortements à 8 semaines de gestation ou moins (Figure 2).
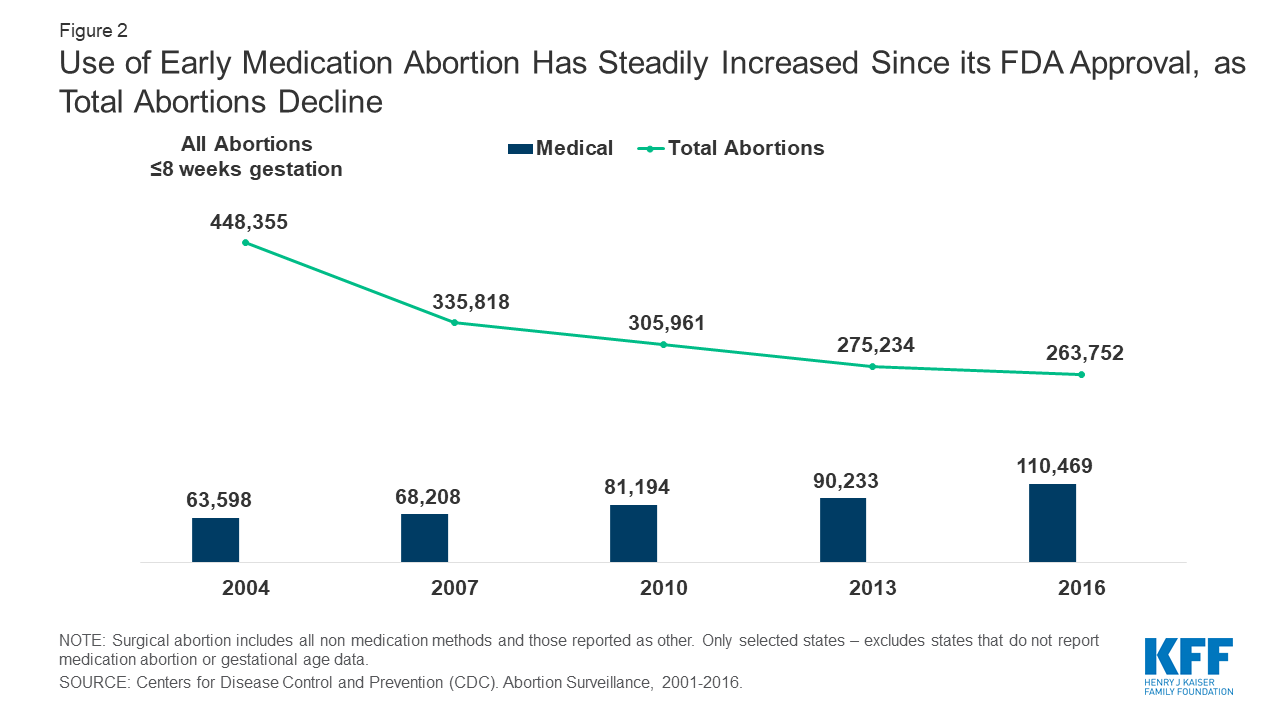
Figure 2 : Le recours à l’avortement médicamenteux précoce a régulièrement augmenté depuis son approbation par la FDA, alors que le nombre total d’avortements diminue
Selon les laboratoires Danco, en 2016, plus de 2,75 millions de femmes aux États-Unis ont utilisé le Mifeprex depuis son approbation par la FDA en 2000. Les données des Centres de contrôle et de prévention des maladies (CDC) montrent que de 2007 à 2016, les avortements déclarés à 8 semaines de gestation ou moins ont augmenté de 2,5%, tandis que les avortements déclarés entre 9 et 13 semaines ont diminué de 7,9%. Un rapport de 2017 du Guttmacher Institute a révélé que les avortements médicamenteux pratiqués jusqu’à 9 semaines de gestation représentaient 39 % de tous les avortements non hospitaliers.
Télémédecine
La télémédecine, ou télésanté, peut être utilisée pour élargir l’accès aux services de santé dans les zones où le nombre de prestataires est limité. De nombreuses femmes, notamment celles qui vivent dans des communautés rurales, doivent parcourir de longues distances pour obtenir des services d’avortement, ce qui a suscité un intérêt pour le potentiel de la télémédecine afin d’élargir l’accès à l’avortement médicamenteux. Parce que la toute nouvelle étiquette de la FDA permet aux femmes de prendre les pilules après avoir quitté la clinique, la télémédecine est apparue comme une option viable pour étendre la disponibilité de l’avortement aux femmes qui sont soit incapables de se rendre à la clinique ou qui, pour d’autres raisons, souhaitent avoir un avortement dans l’intimité de leur propre maison.
Dans le cadre des efforts visant à limiter l’accès à l’avortement, de nombreux États ont pris des mesures pour bloquer l’utilisation de la télémédecine pour l’avortement. Six États, l’Arizona, l’Arkansas, l’Idaho, le Missouri, la Louisiane et la Virginie occidentale, ont adopté des lois interdisant spécifiquement la télémédecine pour la fourniture d’avortements. En outre, 15 autres États ont promulgué des lois qui exigent que le clinicien fournissant une interruption de grossesse médicamenteuse soit physiquement présent pendant la procédure, interdisant de fait l’utilisation de la télémédecine pour délivrer des médicaments pour l’avortement à distance (Figure 3).

Figure 3 : 18 États ont des politiques qui restreignent la télémédecine pour l’avortement médicamenteux
Avortement autogéré
L’avortement autogéré, parfois référencé comme avortement « auto-induit » ou « à domicile », est lorsqu’une personne met fin à une grossesse en dehors du cadre des soins médicaux, généralement en commandant des pilules abortives en ligne. Cette pratique est illégale aux États-Unis, mais est autorisée dans certains autres pays. Les femmes peuvent chercher à gérer elles-mêmes leur avortement pour de nombreuses raisons, notamment les obstacles à l’accès aux cliniques, le coût, le transport et l’intimité. Le coût médian des produits à base de mifepristone-misoprostol commandés en ligne est d’environ 205 dollars, soit la moitié du prix moyen d’un avortement en clinique. Les obstacles juridiques, tels que la menace de poursuites pénales, à l’avortement autogéré affectent les personnes enceintes ainsi que celles qui les aident à mettre fin à leur grossesse.
Women Help Women, qui opère déjà pour fournir des pilules aux femmes dans d’autres pays, a récemment lancé Self-managed Abortion ; Safe and Supported (SASS), pour fournir des informations sur l’avortement médicamenteux autogéré aux femmes aux États-Unis. Cependant, en raison d’obstacles juridiques, ils n’expédient pas de pilules aux femmes des États-Unis. Quelques projets, tels que la campagne Plan C, s’efforcent actuellement d’informer les femmes américaines sur les avortements autogérés, notamment sur la manière de prendre les médicaments de manière appropriée, sur les moyens d’obtenir des fonds pour les payer et sur une liste de détaillants en ligne avec des commentaires sur le prix, le délai de livraison, la qualité du produit et la surveillance des médecins. La FDA a émis des lettres d’avertissement à certaines de ces organisations, dont Aidaccess.org et RAblon, leur demandant de cesser immédiatement l’introduction de médicaments abortifs aux États-Unis, car la mifépristone ne peut être légalement délivrée qu’en utilisant le protocole REMS.
Conclusion
Même si les taux globaux d’avortement diminuent, le recours à l’avortement médicamenteux a considérablement augmenté depuis son approbation par la FDA en 2000. La disponibilité du médicament peut avoir déplacé le moment moyen où les avortements se produisent à un stade plus précoce de la grossesse. Son utilisation a toutefois été limitée par les réglementations fédérales et nationales. Notamment l’exigence du REMS de la FDA, l’interdiction de la télémédecine et l’obligation de délivrer la mifépristone en personne, ainsi que l’obligation d’effectuer des visites de conseil en personne et d’autres tests qui ne sont pas recommandés médicalement pour des raisons de sécurité. Alors que certains États continuent d’imposer des réglementations qui limitent l’accès, d’autres explorent des moyens d’accroître l’accès en autorisant les prestataires cliniques non médecins à prescrire la mifépristone et en testant l’efficacité de la télémédecine pour élargir l’accès aux services d’avortement pour ceux qui le demandent.
Notes de fin
-
A la suite du changement d’étiquette de 2016, le fournisseur n’est plus tenu de remettre à chaque femme une copie du guide de médication du Mifeprex.
← Retour au texte
.
0 commentaire