Los pacientes con una enfermedad que requiere la cooperación de médicos de diferentes especialidades se enfrentan a riesgos debido a la falta de comunicación, a los diferentes objetivos percibidos y a las bases de conocimiento variables entre las subespecialidades. Un ejemplo es la prescripción de hidroxicloroquina por parte de los internistas para las enfermedades autoinmunes y la detección de dosis tóxicas y retinopatía por parte de los oftalmólogos. En este resumen, identificaré las lagunas en la comprensión y la comunicación entre las especialidades que conducen a casos evitables de retinopatía, y discutiré cómo se pueden salvar.
Un problema persistente
¿Por qué se siguen desarrollando casos de retinopatía por hidroxicloroquina, cuando su patogénesis se conoce desde la década de 1980? Entre las diversas causas que contribuyen a ello, la principal es que a demasiados pacientes se les prescriben dosis diarias tóxicas.1 La hidroxicloroquina se almacena en los tejidos magros, y se excluye en gran medida de la grasa.2 Por lo tanto, la dosificación de la HC debe basarse en la masa corporal magra.3 En la mayoría de las personas, esto puede determinarse a partir de tablas de peso corporal ideal (PCI) basadas en la altura. Sin embargo, en los pacientes delgados y asténicos en los que el peso corporal real es inferior al ideal, la dosificación debe basarse en el peso corporal real (PCA), no en el PCI.4 Aunque existen algunos casos, es extremadamente raro que se desarrolle una FC si la dosis diaria no supera los 6,5 mg/kg, basándose en el uso del menor de los pesos corporales reales y del PCI para el denominador.5
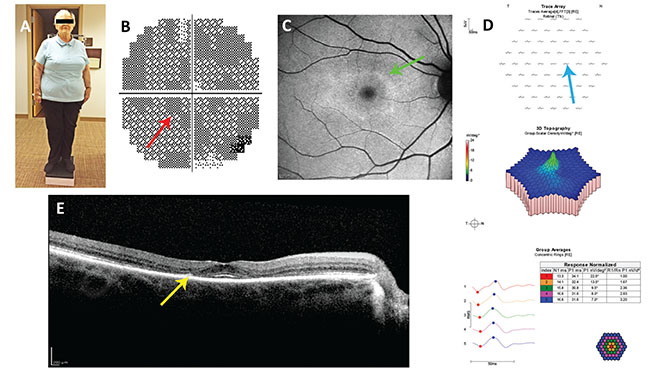
Figura 1. Informe del caso nº 1. A: Obsérvese el somatotipo. En el paciente obeso de baja estatura, la dosificación basada en el peso corporal ideal, no en el peso corporal real, es apropiada. B: Escotoma paracentral (flecha roja) en su prueba de campo visual 10-2 de 2012, omitida por su oftalmólogo. C: Anillo de hiperautofluorescencia (flecha verde) en las imágenes de autofluorescencia del fondo de ojo de 2014. D: Reducción de las amplitudes de las ondas paracentrales (flecha azul) en la electrorretinografía multifocal. E: Pérdida paracentral de la línea elipsoide y adelgazamiento de la capa nuclear externa (flecha amarilla) en la tomografía de coherencia óptica de dominio espectral.
Las publicaciones oftálmicas son parcialmente responsables de la confusión que existe en cuanto a la importancia de la dosis diaria para prevenir la FC. Considere lo que dicen tres conjuntos consecutivos de directrices de la Academia Americana de Oftalmología (Tabla 1): Las directrices de 2002 afirman que la dosis diaria es de «importancia primordial», y aconsejan el uso de ABW excepto en pacientes obesos, en cuyo caso se recomienda IBW. En 2011, las directrices dieron la vuelta, descartando la importancia de la dosis diaria a menos que un paciente sea obeso, en cuyo caso se aconseja la dosificación por IBW. En 2016, las directrices dieron un vuelco, reafirmando la importancia de la dosis diaria, pero descontando la dosificación por IBW mientras se enfatiza la dosificación por ABW e introduciendo un factor de conversión diferente.
Con tal inconsistencia, es fácil entender cómo los reumatólogos y los oftalmólogos pueden estar confundidos sobre la importancia de la dosis diaria y cómo debe ser calculada. Las directrices de 2002 eran potencialmente peligrosas por su falta de especificidad en cuanto a cómo utilizar el ABW o el IBW en el cálculo de la dosis diaria. Las directrices de 2011 eran potencialmente peligrosas para la persona cuyo PCA es inferior al PCI (véase el caso 1). Las directrices de 2016 son peligrosas para la persona obesa en la que el IBW es menor que el ABW (Ver caso 2).
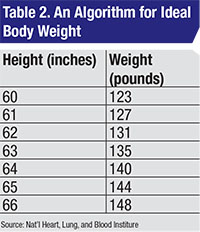
La prescripción segura de hidroxicloroquina no es difícil. Se toma el valor menor del PCA y del PCI en función de la estatura.4 La dosis diaria no debería superar los 6,5 mg/kg/d en función del valor menor del PCA y del PCI. El algoritmo que se debe utilizar para el PCI es controvertido, pero en la práctica probablemente no importe. Yo prefiero el algoritmo del Instituto Nacional del Corazón, los Pulmones y la Sangre (Tabla 2).3
En las siguientes secciones, describiré informes de casos relacionados con la HC y explicaré las cuestiones de dosificación implicadas.
Informe de caso nº 1
Una mujer de 74 años con artritis reumatoide comenzó a tomar hidroxicloroquina 400 mg/día en 2004. Medía 1,5 metros, pesaba 198 libras y no tenía insuficiencia renal ni hepática (Figura 1). Fue remitida por primera vez por su reumatólogo para la detección de retinopatía en 2012, y había perdido el ojo izquierdo por un traumatismo cuando era niña.
El oftalmólogo que la revisó en 2012 la encontró con una agudeza visual corregida de 20/20 en el ojo derecho e interpretó su campo visual 10-2 y su electrorretinograma multifocal como normales, aunque no lo eran. No reconoció su dosis tóxica y no hizo ninguna recomendación para cambiarla. Se le pidió que volviera en seis meses, pero nunca lo hizo.
Un oftalmólogo diferente la examinó en 2014. Su agudeza visual corregida era de 20/20 en el ojo derecho y su examen del fondo de ojo era normal. Una FV 10-2 utilizando un objeto de prueba rojo mostró la progresión de un escotoma anular que estaba presente en 2012. Un estudio de imagen de tomografía de coherencia óptica de dominio espectral de la mácula mostró la pérdida de la zona elipsoide parafoveal y el adelgazamiento de la capa nuclear externa.
Este caso ilustra las siguientes trampas evitables y comúnmente vistas en el manejo multidisciplinario del paciente que toma HC:
– El reumatólogo prescribió una dosis tóxica de HC basada en la altura y el peso del paciente. El paciente medía 1,5 m, con un peso corporal ideal de 55,9 kg (ver Tabla 2) y una dosis máxima diaria segura de 55,9 x 6,5=363 mg/d de HC. Para lograr esto utilizando el tamaño de píldora disponible de 200 mg, se considera el hecho de que la HC tiene una vida media larga (aproximadamente 40 días1). Por lo tanto, se puede omitir un día de dosificación en una semana y llegar a una dosis diaria media adecuada. A lo largo de una semana, este paciente puede tomar hasta 7 x 363=2.543 mg de HC de forma segura. Si toma dos comprimidos al día de lunes a sábado y se salta la HC los domingos, su dosis total semanal será de 2.400 mg, lo que supone una media de 2.400/7=343 mg/día, que es menos que una dosis tóxica.
– La paciente no se sometió a un examen de detección oftalmológica de referencia y no fue enviada a un examen por un oftalmólogo hasta que llevaba ocho años de terapia. Esto ocurrió a pesar de que la paciente tenía un alto riesgo de toxicidad basado en su dosis diaria. Las directrices de la AAO establecen que debe obtenerse un examen de referencia y luego, para los pacientes de bajo riesgo, los exámenes anuales deben comenzar cinco años después. Los oftalmólogos han rechazado regularmente estas recomendaciones.4,7 En lugar de seguir recomendando un vacío en el examen que es rechazado por los encargados de la detección de la retinopatía, sería mejor que las directrices adoptaran la realidad práctica de que el examen anual es la norma, que en los primeros años tiene como objetivo principal detectar y corregir la dosificación diaria tóxica.
– El médico no reconoció ni corrigió la dosificación tóxica de la HC. La dosificación tóxica se encuentra sistemáticamente entre el 12,8 y el 74,7 por ciento de los pacientes que toman HC.4,8-10 La corrección de la dosificación diaria tóxica es la acción más común del oftalmólogo que realiza el cribado, y es la principal razón para cribarse los pacientes que toman HC. Cuando se asume una dosis segura, como en Gran Bretaña, no se recomienda el cribado porque la rareza de la RH en estas circunstancias hace que se desperdicien los escasos recursos.11
– El primer oftalmólogo no reconoció la evidencia de toxicidad en la FV 10-2 inicial. El diagnóstico de RH se basa en pruebas auxiliares: 10-2 VF; SD-OCT; mfERG; y la imagen de autofluorescencia del fondo de ojo. Los oftalmólogos que realizan el cribado de la FC tienen la obligación de entender qué constituye una prueba positiva, cuáles son los posibles artefactos y cómo utilizar las múltiples modalidades para aumentar la confianza clínica en el diagnóstico. El tema se ha explorado a fondo en múltiples publicaciones.1,12,13 El hecho de no interpretar correctamente las pruebas de los pacientes ha sido la base de grandes acuerdos por mala praxis en casos de RH perdidos.
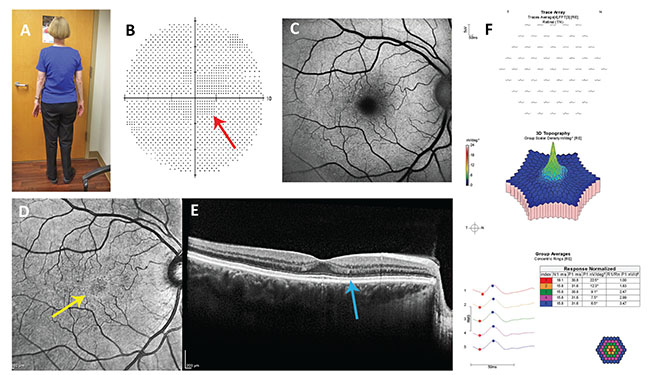
Figura 2. Caso clínico nº 2: A: Obsérvese el somatotipo. En el paciente asténico, la dosificación basada en el peso corporal real, no en el peso corporal ideal, es apropiada. B: El escotoma central no reproducible (flecha roja) en su prueba de campo visual 10-2 no es típico de la retinopatía por hidroxicloroquina. C: La autofluorescencia del fondo de ojo es normal. D: La imagen de reflectancia en el infrarrojo cercano muestra un anillo hiperreflectivo (flecha amarilla) que tiene baja sensibilidad y especificidad para la retinopatía por hidroxicloroquina. E: La reflectividad de la línea elipsoidal en la parafovea es ligeramente menor que en la fóvea, un signo potencialmente temprano de retinopatía. F: La electrorretinografía multifocal es normal.
Informe de caso nº 2
En 2015, un oftalmólogo examinó a una mujer de 63 años con artritis reumatoide que había estado tomando HC 400 mg/d desde 1990 (25 años, 3.650 g de dosis acumulada). Medía 1,5 m. y pesaba 1,5 kg. No tenía ninguna enfermedad renal ni hepática. Su agudeza visual corregida era de 20/20 y su examen del fondo de ojo era normal bilateralmente. Su campo visual 10-2 realizado con un objeto de prueba rojo mostró un escotoma central relativo no reproducible (Figura 2). La autofluorescencia del fondo de ojo era normal. Las imágenes de reflectancia en el infrarrojo cercano mostraron un débil anillo hiperreflectante, que se ha asociado inconsistentemente con la FC temprana.14 La SD-OCT mostró una línea elipsoide ligeramente menos hiperreflectante y una sugerencia de adelgazamiento de la capa nuclear externa. La electrorretinografía multifocal fue normal.
Debido a que no había retinopatía definida, se le autorizó a seguir usando HC, pero se corrigió su dosis tóxica. El menor de los valores de su PCA y PCI fue su PCA, que era de 112 libras. Por lo tanto, el límite superior de su dosis diaria segura era de 330 mg. Se recomendó que no tomara más de 200 mg/día durante los siguientes seis meses, momento en el que se recomendó repetir las pruebas auxiliares para determinar si había una señal de retinopatía temprana dada su gran dosis acumulada.
Las publicaciones reumatológicas también contribuyen a la confusión sobre la dosis. En un artículo en línea de abril del sitio web de reumatología RheumNow.com, la autora escribe: «Los factores de riesgo conocidos para el desarrollo de depósitos oculares incluyen la duración de la terapia, la dosis acumulada y la función renal».15 No menciona el factor de riesgo más importante, y el único modificable: la dosis diaria. Continúa escribiendo: «La Academia Americana de Oftalmología (AAO) aconseja una dosis basada en el peso de 6,5 mg/kg, con un límite máximo de 400 mg/día. Las excepciones son los individuos de baja estatura y los pacientes obesos, para los que la AAO aconseja calcular la dosis basándose en el peso corporal ideal para la estatura». Sin embargo, esto no es lo que afirma la referencia citada. Por el contrario, afirma: «La recomendación anterior hacía hincapié en la dosificación según el peso. Sin embargo, la mayoría de los pacientes reciben rutinariamente 400 mg de HCQ al día. …Esta dosis se considera ahora aceptable, excepto en el caso de los individuos de baja estatura, para los que la dosis debe determinarse en función del peso corporal ideal para evitar la sobredosis».16
El autor continúa: «La sensibilidad y especificidad de estas pruebas aún no se conocen para la toxicidad retiniana relacionada con la hidroxicloroquina. Hay una alta tasa de anormalidades de base, en particular en aquellos que son ancianos o tienen enfermedades comórbidas, que hacen que los cambios sean difíciles de interpretar. Otra cuestión es que el propio lupus eritematoso sistémico se asocia a la presencia de anomalías en la retina, lo que aumenta la complejidad de descifrar estas pruebas.» Estas afirmaciones son incorrectas. La sensibilidad y especificidad relativas de las pruebas son conocidas (la mfERG es la más sensible, la 10-2 VF la siguiente y la SD-OCT la menor; la SD-OCT es la más específica, la 10-2 VF la siguiente y la mfERG la menor)17 . El LES rara vez afecta a ninguna de las pruebas.

Por último, el autor aboga por una dosificación basada en 6,5 mg/kg/peso corporal real. Esta es una recomendación peligrosa para el paciente de baja estatura y obeso, como se ejemplifica en el Informe de Caso 1.
En una revisión reumatológica de la HC los autores escribieron: «Un estudio francés demostró que la concentración de HC en sangre total >1.000 ng/ml reducía el riesgo de brotes de lupus. La medición de los niveles de HC en sangre puede sugerir que algunos pacientes necesitan >6,5 mg/kg/día para alcanzar el nivel recomendado. Estos pacientes no deberían tener un mayor riesgo de toxicidad, siempre que se controlen los niveles, pero puede ser importante controlar también la dosis acumulada al evaluar el riesgo de toxicidad ocular».18 La declaración sugiere erróneamente que existe una relación conocida entre los niveles de HC en sangre y la FC, pero no es así.
Si los internistas que prescriben y los oftalmólogos que realizan las revisiones pusieran en práctica un conocimiento más claro de la dosis diaria correcta, la prevalencia de la FC disminuiría. En la mayoría de los casos, la enfermedad es iatrogénica y puede evitarse. La dosificación diaria es el único factor de riesgo modificable y merece la mayor atención en las visitas de cribado, especialmente en los primeros cinco años de uso del fármaco, antes de que la carga irreversible y acumulativa se haya acumulado y eleve el riesgo de retinopatía. La recomendación de omitir el cribado en los casos de bajo riesgo durante los cinco años posteriores a un examen inicial ha sido ampliamente rechazada por quienes realizan el cribado, y es probablemente errónea dada la alta prevalencia de la dosificación tóxica. La detección y corrección de la dosificación tóxica es de gran valor para la prevención de la retinopatía en los primeros años de toma de HC. Los casos extremadamente raros que desarrollan retinopatía a pesar de una dosificación segura tienen más probabilidades de ser detectados cuando se utiliza conjuntamente una prueba auxiliar más sensible y más específica, por ejemplo, 10-2 VF y SD-OCT, y cuando la interpretación se realiza de forma competente.
El Dr. Browning es especialista en retina en Charlotte Eye, Ear, Nose, and Throat Associates. Contacte con el Dr. Browning en 6035 Fairview Rd, Charlotte, NC 28210. Se puede contactar con él en el (704)-295-3180, o en [email protected].
1. Browning DJ. Hydroxychloroquine and chloroquine retinopathy. Nueva York: Springer, 2014.
2. McChesney EW, Banks WF Jr, Fabian RJ. Tissue distribution of chloroquine, hydroxychloroquine, and desethylchloroquine in the rat. Toxic App Pharm 1967;10:501-513.
3. Browning DJ, Lee C, Rotberg D. El impacto de diferentes algoritmos para el peso corporal ideal en la detección de la retinopatía por hidroxicloroquina en las mujeres. Clinical Ophthalmology 2014;8:1401.
4. Browning DJ. Impacto de las directrices revisadas de la Academia Americana de Oftalmología respecto al cribado de hidroxicloroquina en la práctica real. Am J Ophthalmol 2013;155:418..
5. Falcone PM, Paolini L, Lou PL. Toxicidad por hidroxicloroquina a pesar de la terapia a dosis normales. Ann Ophthalmol 1993;25:385-388.
6. Browning DJ. Respuesta a Definir el peso corporal ideal. Am J Ophthalmol 2002;134:935-936.
7. Blomquist PH, Chundru RK. Screening for hydroxychloroquine toxicity by Texas ophthalmologists. J Rheumatol 2002;29:1665.
8. Wolfe F, Marmor MF. Tasas y predictores de toxicidad retiniana por hidroxicloroquina en pacientes con artritis reumatoide y lupus eritematoso sistémico. Arthritis Care Res 2010;62:775-784.
9. Cukras C, Huynh N, vitale S, Wong WT, Ferris III FL, Sieving PA. Pruebas de cribado subjetivas y objetivas para la toxicidad de la hidroxicloroquina. Ophthalmology 2015;122:356-366.
10. Lee MG, Kim SJ, Ham DI, Kang SW, Kee C, Lee J, Cha HS, Koh EM. Macular ganglion cell-inner plexiform layer thickness in patients on hydroxychloroquine therapy. Invest Ophthalmol Vis Sci 2015;56:396-402.
11. FielderA, Graham E, Jones S, et al. Royal college of ophthalmologists guidelines: Toxicidad ocular e hidroxicloroquina. Eye 1998;12:907-909.
12. Marmor MF, Melles RB. Disparidad entre los campos visuales y la tomografía de coherencia óptica en la retinopatía por hidroxicloroquina. Ophthalmology 2014;121:1257-1262.
13. Mititelu M, Wong BJ, Brenner M, et al. Progresión de los efectos tóxicos de la hidroxicloroquina tras el cese del tratamiento farmacológico. Nueva evidencia de la imagen multimodal. Arch Ophthalmol 2013;131:1187-1197.
14. Wong KL, Pautler SE, Browning DJ. Maculopatía de ojo de buey de reflectancia en el infrarrojo cercano como indicador temprano de toxicidad por hidroxicloroquina. Clin Ophthalmol 2015; 9:521-5.
15. Petrie M, Durcan L. «The role of hydroxychloroquine blood levels in SLE» found at http://rheumnow.com/blog/role-hydroxychloroquine-blood-levels-sle#.VvaKbIfbwMQ.mailto. Consultado el 28 de septiembre de 2016.
16. Marmor MF, Kellner U, Lai TYY, Lyons JS, Mieler WF. Recomendaciones revisadas sobre el cribado de la retinopatía por cloroquina e hidroxicloroquina. Ophthalmology 2011;118:415.
17. Browning DJ, Lee C. La sensibilidad y especificidad relativa de los campos visuales 10-2, la electrorretinografía multifocal y la tomografía de coherencia óptica de dominio espectral en la detección de la retinopatía por hidroxicloroquina y cloroquina. Clinical Ophthalmology 2014;8:1389-1399.
18. Ding HJ, Denniston AK, Rao VK, Gordon C. Retinopatía relacionada con la hidroxicloroquina. Rheumatology (Oxford) 2016;55:6:957-67.
0 comentarios