 El aluminio se ha utilizado en Estados Unidos durante más de 100 años. En una época, se consideraba más valioso que el oro, ya que tardaba mucho en refinarse y producirse. La primera versión pura del metal apareció en 1825, mientras que los métodos rentables aparecieron en 1889. A medida que el aluminio se hizo más común, se utilizó en una variedad de formas, desde el cableado eléctrico hasta los motores. En el siglo XX se produjeron avances muy rápidos en su utilidad. Con el desarrollo de aleaciones que mejoraron sus propiedades físicas, se le dio un mayor uso en varias industrias.
El aluminio se ha utilizado en Estados Unidos durante más de 100 años. En una época, se consideraba más valioso que el oro, ya que tardaba mucho en refinarse y producirse. La primera versión pura del metal apareció en 1825, mientras que los métodos rentables aparecieron en 1889. A medida que el aluminio se hizo más común, se utilizó en una variedad de formas, desde el cableado eléctrico hasta los motores. En el siglo XX se produjeron avances muy rápidos en su utilidad. Con el desarrollo de aleaciones que mejoraron sus propiedades físicas, se le dio un mayor uso en varias industrias.
El aluminio es uno de los elementos metálicos más comunes que se encuentran en la Tierra, con un 8% de la corteza, sólo superado por el silicio. Se encuentra en compuestos químicos mezclados con otros elementos como el azufre, el silicio y el oxígeno. La fórmula química del aluminio es Al2O3. El aluminio puro se produce a partir del mineral de óxido de aluminio, que se extrae de la arcilla. La bauxita contiene la mayor cantidad del óxido, entre el 45 y el 60%, y es fácilmente accesible en la tierra blanda.
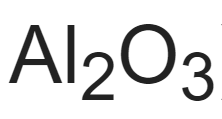
La producción de aluminio comienza con el hidróxido de sodio que disuelve el compuesto de aluminio de la bauxita para eliminar las impurezas. La criolita se utiliza como electrolito en el proceso de fundición con la ayuda del fluoruro de aluminio para ayudar a bajar el punto de fusión de la criolita. Una vez que la mezcla alcanza la temperatura adecuada, se introducen electrodos de carbono para transmitir una corriente eléctrica a través del electrolito. La electricidad es el mayor gasto del proceso de fabricación del aluminio, ya que requiere 15 kWh de energía por cada dos libras de aluminio.
En la producción de aluminio se utilizan dos procesos: Bayer y Hall-Heroult. Mientras que el método Bayer trabaja con el mineral de bauxita, el proceso Hall-Heroult utiliza un subproducto del método Bayer. El proceso Bayer comienza triturando y calentando la bauxita. La solución calentada pasa por una serie de tanques para separar el óxido de aluminio. El proceso Hall-Heroult comienza con la alúmina, un subproducto del método Bayer. Los cristales de alúmina, que pueden ser un polvo o una sal, se disuelven en la solución de criolita.
Aunque la alúmina es un subproducto, es importante en la fabricación de varios productos domésticos e industriales. Aproximadamente el diez por ciento se reutiliza para una larga lista de otros usos, desde el detergente para la ropa hasta los parabrisas cerámicos transparentes para los aviones. Un uso especialmente interesante es el refinado de combustible para el transbordador espacial.
Los usos del aluminio son infinitos e incluyen latas, papel de aluminio, herramientas de cocina, marcos de ventanas, barriles de cerveza, piezas de aviones, etc. Se puede fundir y mecanizar fácilmente en formas incalculables. Una de sus principales características es su resistencia a la corrosión, que le confiere una vida más larga. En la mayoría de los casos, se utiliza como aleación, ya que en su forma pura carece de resistencia. El cobre, el manganeso, el magnesio y el silicio son las aleaciones más comunes, ya que aumentan la resistencia del aluminio pero mantienen su ligereza. Como el aluminio cuesta menos que el cobre y es un buen conductor eléctrico, se utiliza para fabricar cables eléctricos.
Con la mejora de los métodos de producción, el aluminio se ha convertido en un componente fundamental en la fabricación de productos comerciales e industriales modernos. La sociedad ha llegado a confiar en él por su apariencia y flexibilidad.
0 comentarios