Objetivos de aprendizaje
- Aprender algunas aplicaciones de la radiactividad.
Los isótopos radiactivos tienen una gran variedad de aplicaciones. Generalmente, sin embargo, son útiles porque podemos detectar su radiactividad o podemos utilizar la energía que liberan.
Los isótopos radiactivos son trazadores eficaces porque su radiactividad es fácil de detectar. Un trazador es una sustancia que puede utilizarse para seguir el camino de esa sustancia a través de alguna estructura. Por ejemplo, las fugas en las tuberías de agua subterráneas pueden descubrirse haciendo correr un poco de agua que contenga tritio a través de las tuberías y luego utilizando un contador Geiger para localizar cualquier tritio radiactivo presente posteriormente en el suelo alrededor de las tuberías. (Recordemos que el tritio, 3H, es un isótopo radiactivo del hidrógeno.)
Los trazadores también pueden utilizarse para seguir los pasos de una reacción química compleja. Después de incorporar átomos radiactivos a las moléculas reactivas, los científicos pueden rastrear dónde van los átomos siguiendo su radiactividad. Un excelente ejemplo de ello es el uso del carbono 14 radiactivo para determinar los pasos de la fotosíntesis en las plantas. Conocemos estos pasos porque los investigadores siguieron el progreso del carbono-14 radiactivo a lo largo del proceso.
Los isótopos radiactivos son útiles para establecer las edades de diversos objetos. La vida media de los isótopos radiactivos no se ve afectada por ningún factor ambiental, por lo que el isótopo actúa como un reloj interno. Por ejemplo, si se analiza una roca y se descubre que contiene una determinada cantidad de uranio 235 y una determinada cantidad de su isótopo hijo, podemos concluir que una determinada fracción del uranio 235 original ha decaído radiactivamente. Si la mitad del uranio se ha descompuesto, entonces la roca tiene una edad de una semivida del uranio-235, o sea, unos 4,5 × 109 años. Muchos análisis como éste, que utilizan una amplia variedad de isótopos, han indicado que la edad de la propia Tierra es superior a 4 × 109 años. En otro interesante ejemplo de datación radiactiva, la datación por 3H se ha utilizado para verificar las añadas declaradas de algunos vinos finos antiguos.
El carbono-14 (su vida media es de 5.370 y) es especialmente útil para determinar la edad de artefactos que alguna vez estuvieron vivos (por ejemplo, materia animal o vegetal). Una pequeña cantidad de carbono-14 se produce de forma natural en las capas superiores de la atmósfera, y los seres vivos incorporan parte de él en sus tejidos, acumulándose hasta un nivel constante, aunque muy bajo. Sin embargo, una vez que un ser vivo muere, ya no adquiere carbono-14 y, con el paso del tiempo, el carbono-14 que había en los tejidos se descompone. Si se descubre un artefacto que estuvo vivo y se analiza muchos años después de su muerte, con el carbono-14 restante comparado con el nivel constante conocido, se puede determinar una edad aproximada del artefacto. Utilizando estos métodos, los científicos determinaron que la edad del Sudario de Turín (hecho de lino, que proviene de la planta de lino, y que algunos pretenden que sea el paño de enterramiento de Jesucristo; Figura \(\PageIndex{1})) es de unos 600-700 años, y no de 2.000 años como afirman algunos. Los científicos también pudieron utilizar la datación por radiocarbono para demostrar que la edad de un cuerpo momificado encontrado en el hielo de los Alpes era de 5.300 años.
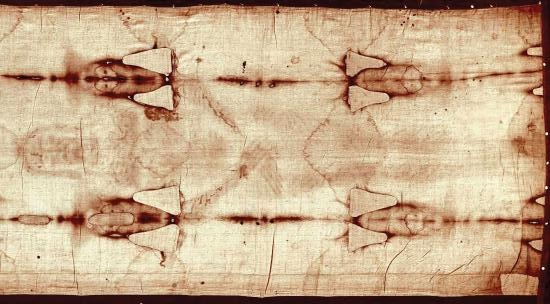
Figura \(\PageIndex{1}): Sábana Santa de Turín. En 1989, varios grupos de científicos utilizaron la datación por carbono 14 para demostrar que la edad de la Sábana Santa era de sólo 600-700 años. Muchas personas siguen aferrándose a una noción diferente, a pesar de las pruebas científicas.
La radiación emitida por algunas sustancias radiactivas puede utilizarse para matar microorganismos en una variedad de alimentos, lo que prolonga la vida útil de estos productos. Productos como los tomates, las setas, los brotes y las bayas se irradian con las emisiones de cobalto-60 o cesio-137. Esta exposición mata muchas de las bacterias que causan el deterioro, por lo que los productos se mantienen frescos durante más tiempo. Los huevos y algunas carnes, como la de vaca, cerdo y aves, también pueden irradiarse. Al contrario de lo que creen algunas personas, la irradiación de los alimentos no hace que éstos sean radiactivos.
Los isótopos radiactivos tienen numerosas aplicaciones médicas: diagnosticar y tratar enfermedades. Un ejemplo de aplicación diagnóstica es el uso de yodo-131 radiactivo para analizar la actividad de la tiroides (Figura \(\PageIndex{2}\)). La glándula tiroidea, situada en el cuello, es uno de los pocos lugares del cuerpo con una concentración significativa de yodo. Para evaluar la actividad tiroidea, se administra una dosis medida de yodo-131 a un paciente, y al día siguiente se utiliza un escáner para medir la cantidad de radiactividad en la glándula tiroidea. La cantidad de yodo radiactivo que se acumula allí está directamente relacionada con la actividad del tiroides, lo que permite a los médicos capacitados diagnosticar tanto el hipertiroidismo como el hipotiroidismo. El yodo 131 tiene una vida media de sólo 8 días, por lo que el potencial de daño debido a la exposición es mínimo. El tecnecio-99 también puede utilizarse para comprobar la función tiroidea. Los huesos, el corazón, el cerebro, el hígado, los pulmones y muchos otros órganos pueden visualizarse de forma similar utilizando el isótopo radiactivo apropiado.
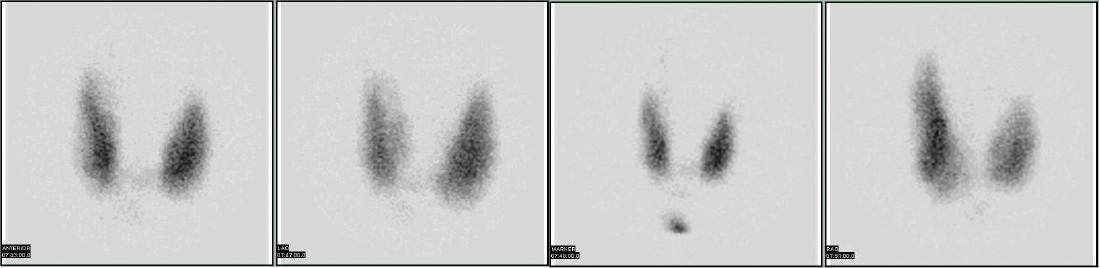
Figura \N(\PageIndex{2}\N-): Diagnóstico médico. El yodo radiactivo puede utilizarse para obtener imágenes de la glándula tiroides con fines de diagnóstico. Fuente: Escaneo por cortesía de Myo Han, http://en.Wikipedia.org/wiki/File:Thyroid_scan.jpg.
En estas técnicas de diagnóstico se necesita muy poco material radiactivo porque la radiación emitida es muy fácil de detectar. Sin embargo, las aplicaciones terapéuticas suelen requerir dosis mucho mayores porque su objetivo es matar preferentemente los tejidos enfermos. Por ejemplo, si se detecta un tumor de tiroides, una infusión mucho mayor (miles de rem, frente a una dosis de diagnóstico de menos de 40 rem) de yodo-131 podría ayudar a destruir las células tumorales. Del mismo modo, el estroncio radiactivo se utiliza no sólo para detectar sino también para aliviar el dolor de los cánceres óseos. En la tabla \(\PageIndex{1}) se enumeran varios isótopos radiactivos y sus usos médicos.
| Isótopo | Uso |
|---|---|
| 32P | Detección y tratamiento del cáncer, especialmente en ojos y piel | 59Fe | diagnóstico de la anemia | 60Co | irradiación de tumores con rayos gamma |
| 99mTc | cerebro, tiroides, hígado, médula ósea, pulmón, corazón y exploración intestinal; determinación del volumen sanguíneo |
| 131I | diagnóstico y tratamiento de la función tiroidea |
| 133Xe | imagen pulmonar |
| 198Au | diagnóstico de enfermedades de la hígado |
Además de la aplicación directa de isótopos radiactivos al tejido enfermo, las emisiones de rayos gamma de algunos isótopos pueden dirigirse hacia el tejido a destruir. El cobalto-60 es un isótopo útil para este tipo de procedimiento.
Una forma relativamente rara de radiactividad se llama emisión de positrones. Es similar a la emisión de partículas beta, excepto que en lugar de emitir un electrón, un núcleo emite un electrón con carga positiva, llamado positrón. Un positrón es en realidad una pieza de antimateria; por lo tanto, cuando un positrón se encuentra con un electrón, ambas partículas se convierten en radiación gamma de alta energía.
Los isótopos que emiten positrones pueden emplearse en una técnica de imagen médica llamada tomografía por emisión de positrones (PET). Un paciente recibe un compuesto que contiene un isótopo emisor de positrones, ya sea por vía intravenosa o por ingestión. El compuesto radiactivo viaja por todo el cuerpo y, a continuación, el paciente es empujado lentamente a través de un anillo de sensores que detectan la radiación gamma emitida por la aniquilación de positrones y electrones. Un ordenador conectado a los sensores construye una imagen tridimensional del interior de una parte o de todo el cuerpo del paciente, lo que permite a los médicos ver órganos o tumores o regular el funcionamiento de varios órganos (como el cerebro o el corazón) para diagnosticar el estado médico del paciente.
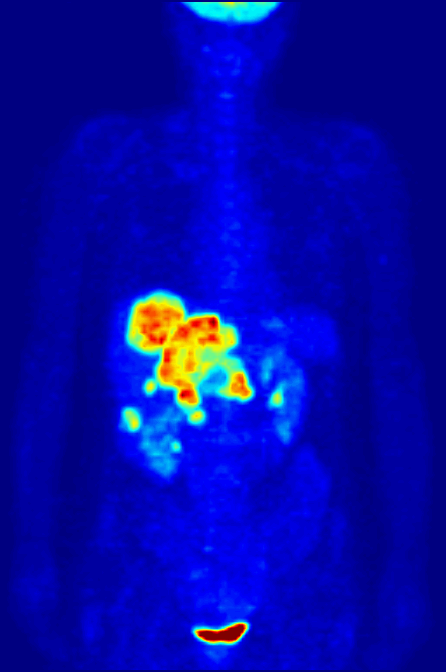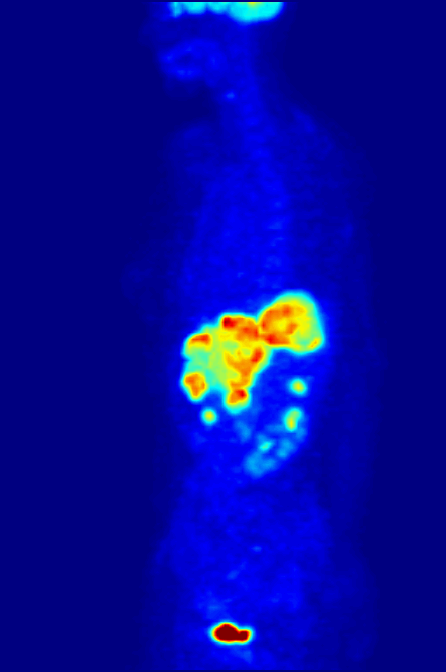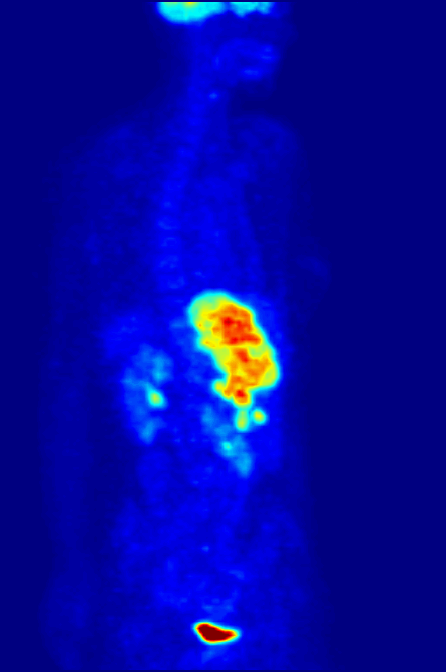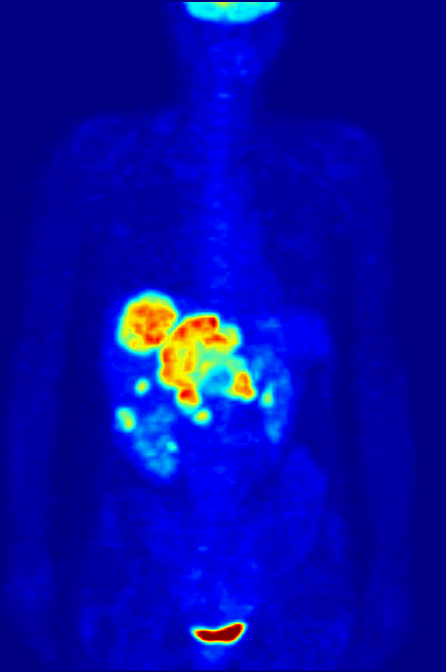
Figura \N(\PageIndex{3}\N): (izquierda) Aparato combinado para tomografía por emisión de positrones (PET) y tomografía computarizada (TC) de rayos X, Siemens Biograph (derecha) Exploración PET de cuerpo entero utilizando 18F-FDG. Imágenes utilizadas con permiso de Wikipedia.
Dos isótopos que sufren emisión de positrones son el carbono-11 y el flúor-18, con vidas medias de 20,4 y 110 minutos, respectivamente. Ambos isótopos pueden incorporarse a moléculas de azúcar e introducirse en el organismo. Los médicos pueden utilizar la intensidad de la emisión de rayos gamma para encontrar tejidos que metabolizan el azúcar más rápidamente que otros tejidos; el tejido de rápida metabolización es un signo de tumor maligno (es decir, canceroso). Los investigadores utilizan técnicas similares para mapear las áreas del cerebro que son más activas durante tareas específicas, como leer o hablar.
La PET es uno de los muchos métodos de diagnóstico y tratamiento que los médicos utilizan para mejorar nuestra calidad de vida. Es uno de los muchos usos positivos de la radiactividad en la sociedad.
Las claves para aprender
- La radiactividad tiene varias aplicaciones prácticas, como los trazadores, las aplicaciones médicas, la datación de objetos que alguna vez estuvieron vivos y la conservación de alimentos.
Contribuidores y atribuciones
-
Anónimo
0 comentarios