US Pharm. 2011;36(4):HS2-HS6.
Neuropatias ópticas são perturbações do nervo óptico envolvendo degeneração do nervo.1 A neuropatia óptica não deve ser confundida com a neurite óptica. Ambas podem levar a problemas de visão; a neurite óptica envolve inflamação do nervo óptico enquanto que a neuropatia óptica se refere a danos de qualquer causa. A neurite óptica é uma das muitas causas da neuropatia óptica.
Neuropatias ópticas podem ser hereditárias ou adquiridas. As etiologias adquiridas da neuropatia óptica incluem tipos isquémicos, nutricionais e tóxicos.1,2 A neuropatia óptica induzida por drogas é do tipo tóxico. Os mecanismos da neuropatia óptica induzida por drogas incluem disfunção mitocondrial, perturbação do fluxo sanguíneo ao nervo óptico, e mecanismos desconhecidos.2
Os sintomas comuns da neuropatia óptica incluem diminuição da visão no campo central, que é tipicamente bilateral mas pode ser unilateral em alguns casos; defeitos do campo visual; e inchaço do nervo óptico.3 O início é tipicamente lento e indolor.2
Na neuropatia óptica induzida por fármacos, a desintoxicação (retirada) do fármaco ofensivo pode levar ao alívio dos sintomas.3,4 Uma vez que muitos dos fármacos conhecidos por causar neuropatia óptica são comuns, é importante que os farmacêuticos estejam cientes deste efeito adverso, a fim de encaminhar atempadamente os pacientes com estes sintomas e evitar danos adicionais e permanentes.
Fármacos que podem causar neuropatia óptica
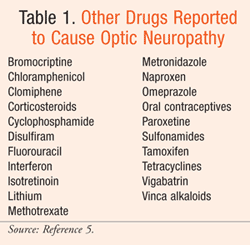
Muitos medicamentos habitualmente prescritos têm sido implicados na neuropatia óptica. Aqui discutidos são os agentes que têm mais informação de apoio: inibidores da fosfodiesterase tipo 5 (PDE-5), amiodarona, linezolida, etambutol, e isoniazida. Outros fármacos que se refere terem causado neuropatia óptica estão listados na TABELA 1.5
Inibidores PDE-5: Esta classe de medicamentos revolucionou o tratamento da disfunção eréctil (DE) nos homens. Actualmente existem três agentes disponíveis – sildenafil (Viagra), tadalafil (Cialis), e vardenafil (Levitra). Eles exercem a sua acção inibindo selectivamente o PDE tipo 5. Considerados agentes de primeira linha para o tratamento da DE, são muito comumente prescritos, com aproximadamente 40 milhões de homens em todo o mundo a serem tratados para disfunção sexual com inibidores da PDE-5.6 Embora a sildenafila, tadalafila e vardenafila sejam específicos para a PDE 5, estes agentes têm demonstrado ter efeitos inibidores sobre a PDE 6, uma isoenzima expressa nas hastes e cones do olho. É teorizado que a inibição da PDE 6 resulta nos muitos distúrbios visuais associados a esta classe de drogas.7-9 Os inibidores da PDE-5 são responsáveis por aproximadamente 19% dos relatórios da FDA sobre toxicidade ocular associada a drogas, tornando-a a classe de drogas mais comumente relatada associada a esta toxicidade.10
NAION: A vigilância pós-comercialização ligou os inibidores da PDE-5 à neuropatia isquémica anterior não artérica (NAION). Esta potencial relação tem suscitado controvérsia. Desde 2000, foram publicados pelo menos 20 relatos de casos na literatura descrevendo o uso de inibidores de PDE-5 e suspeitas de NAION.11,12 A maior parte da literatura publicada está relacionada com o uso de sildenafila desde que este foi o primeiro agente desta classe a ser comercializado (a sildenafila foi introduzida em 1998, 5 anos antes da tadalafila e da vardenafila). Até à data, não foram publicados relatórios de casos envolvendo a vardenafila.
NAION é uma desordem ocular bastante incomum na população em geral que ocorre subitamente, é geralmente indolor, e resulta numa perda parcial irreversível da visão.11,13 Embora seja a neuropatia óptica aguda mais comum em pessoas com mais de 50 anos de idade, há apenas entre 1.500 e 6.000 casos relatados anualmente nos Estados Unidos.14 A etiologia da NAION não é bem compreendida, mas acredita-se que seja causada por uma escassez de fornecimento de sangue ao nervo óptico. Um factor de risco bem estabelecido para o desenvolvimento de NAION ocorre em indivíduos que têm um disco pequeno e um copo fisiológico pequeno ou ausente (isto é, quando o nervo óptico é quase tão grande como a abertura na parte de trás do olho e o disco óptico parece “apinhado”), também conhecido como disco em risco ou disco apinhado. Outros factores de risco associados incluem diabetes, hipertensão, hipercolesterolemia, aterosclerose, doença isquémica do coração, apneia do sono, e hipotensão nocturna. Muitos destes factores de risco estão também associados a ED.8,11
Dos casos notificados NAION, a maioria ocorreu dentro de 24 horas após a administração, geralmente ao acordar pela manhã. Os pacientes apresentaram visão turva e perda de campo visual.15 Além disso, descobriu-se que a maioria dos pacientes tinha discos apinhados como factor de risco juntamente com várias doenças cardiovasculares, que são consideradas como factores de risco tanto para a NAION como para a DE.
Num estudo de coorte retrospectivo que utilizou as bases de dados clínicas e farmacêuticas da National Veterans Health Administration de 2004 a 2005, foi avaliada uma coorte de 2 anos de homens (aproximadamente 4 milhões) que tinham pelo menos 50 anos de idade sem antecedentes de doença do nervo óptico.16 Aproximadamente 11,5% destes pacientes receberam um inibidor de PDE-5; a maioria foi prescrita sildenafil 100 mg. Desta coorte, 0,09% dos doentes tiveram um diagnóstico de nova neuropatia isquémica óptica, com um risco relativo de 1,02 (intervalo de confiança de 95% , 0,92-1,12).
Outro estudo retrospectivo avaliou 38 homens com NAION e comparou-os com 38 homens sem historial da doença.17 Não houve uma diferença global marcada no uso de inibidor de PDE-5 em nenhum dos grupos; contudo, observou-se uma associação significativa para os doentes com historial de enfarte do miocárdio e uso de inibidor de PDE-5 e a ocorrência de NAION (P = .04). Do mesmo modo, a incidência de NAION foi maior nos doentes com historial de hipertensão e uso de inibidor de PDE-5, embora isto não tenha sido significativo (P = .07).17
O mecanismo de acção deste efeito adverso dos inibidores de PDE-5 não é bem compreendido, e isto deve-se em parte ao facto de o mecanismo de acção para o desenvolvimento de NAION não ser totalmente compreendido. Tem sido sugerido que a hipotensão nocturna pode desempenhar um papel no desenvolvimento de NAION, e os inibidores de PDE-5 podem aumentar este efeito, resultando, em última análise, em isquemia do nervo óptico.12,13,18
A incidência de casos de NAION de homens que utilizam inibidores de PDE-5 em todo o mundo é consistente com a da população geral dos EUA.14 A Organização Mundial de Saúde (OMS) e a FDA identificaram a associação de inibidores de NAION e PDE-5 como “possível” causalidade. Um evento adverso “possível” ocorre “dentro de um período de tempo razoável após a administração do medicamento, mas também pode ser explicado por doença concorrente ou outros medicamentos ou produtos químicos. Nesta categoria, faltam ou não são claros os dados positivos de dechallenge”.2 Em 2005, a FDA recomendou que a rotulagem do produto fosse actualizada para conter uma declaração descrevendo esta associação temporal com o uso de inibidores de PDE-5. Até à data, não existem provas convincentes que sugiram que a utilização de inibidores da PDE-5 esteja associada a uma maior incidência de NAION.
Os doentes que tenham experimentado um episódio de NAION devem evitar o uso de inibidores de PDE-5, uma vez que tais indivíduos podem ser susceptíveis de desenvolver NAION no olho contralateral.13,19,20 Alguns oftalmologistas conservadores podem também recomendar que se evite a utilização destes agentes nos doentes que têm um pequeno disco em risco, um critério que pode exigir que todos os doentes façam um exame oftalmológico antes do início do tratamento.13 Os doentes que estão a utilizar inibidores de PDE-5 devem ser aconselhados sobre o risco de desenvolvimento de NAION. Se notarem qualquer perda súbita de visão, devem parar a utilização do inibidor de PDE-5 e procurar atenção médica imediatamente. Todas as incidências devem também ser comunicadas à FDA, incluindo informação sobre duração e dose do medicamento, tempo desde a ingestão do inibidor de PDE-5 até ao início dos resultados, e quaisquer resultados de exames oftalmológicos.19
Amiodarona: Este medicamento, um agente antiarrítmico classe III utilizado principalmente para arritmias ventriculares, tem estado implicado em vários tipos de alterações da visão, incluindo anomalias da córnea, efeitos conjuntivos e neuropatia óptica, mas o mecanismo exacto da neuropatia óptica é desconhecido.21 Foram relatadas alterações visuais com uma prevalência variável de 0% a 11,4% em doentes que tomam este medicamento; a neuropatia óptica foi encontrada num estudo para ocorrer em 1,79% dos doentes.20 A condição é tipicamente insidiosa no início, leva meses a resolver e apresenta-se bilateralmente.4,21,22 Tem-se notado que a neuropatia óptica induzida por amiodarona é muito semelhante à NAION, mas difere dela na medida em que a NAION normalmente apresenta um início rápido, resolução rápida e apresentação unilateral.4,21 Distinguir NAION da neuropatia óptica induzida por amiodarona é muitas vezes difícil.20
A informação de prescrição de amiodarona recomenda exames oftalmológicos regulares, incluindo na linha de base e depois de 6 em 6 meses, para pacientes que recebem o medicamento.4,23 Alguns autores sugeriram que se podem justificar exames oftalmológicos mais frequentes, de 4 em 4 meses até um ano após o início do tratamento.21 Como agente antiarrítmico, a amiodarona não é frequentemente permutável com outros medicamentos, e a decisão de mudar de terapia deve ser feita em consulta com o oftalmologista e cardiologista do paciente.
Linezolida: Este antibiótico oxazolidinona é utilizado para a sua eficácia contra organismos gram-positivos, especificamente Staphylococcus aureus resistente à meticilina (MRSA). A sua segurança global foi demonstrada em ensaios clínicos de até 28 dias de tratamento. A neuropatia óptica tem sido associada à utilização a longo prazo de linezolida, com duração relatada de tratamento que varia entre 5 a 11 meses em doses de 600 a 1.200 mg/dia, bem fora da duração do ensaio clínico estudado de 28 dias ou menos.4,24 Contudo, a literatura mais recente relata neuropatia óptica após uma duração mais curta de tratamento de apenas 16 dias.25,26
Os sintomas são graduais, e há um início indolor de perda bilateral de visão. A interrupção do linezolida levou a uma melhoria dos sintomas visuais em todos os casos relatados. O mecanismo da neuropatia óptica induzida por linezolida não é conhecido, mas pode dever-se à toxicidade mitocondrial da ligação ao rRNA 16S mitocondrial.27 A linezolida penetra bem no sistema nervoso central e nos olhos, o que pode levar a uma neurotoxicidade reforçada.24,28 A retirada de linezolida e a mudança de terapia antibacteriana para outro agente pode ajudar à recuperação, embora em alguns casos possa ser necessária a continuação da linezolida para tratar adequadamente certas infecções.2 Recomenda-se a realização de exames oftalmológicos de base e periódicos para os pacientes que recebem tratamento linezolidário a longo prazo.4
Ethambutol: Este medicamento, um agente de primeira linha no tratamento e prevenção da tuberculose, causa numerosos efeitos adversos oculares. Tem sido bem documentado causar neuropatia óptica em até 5% dos pacientes que tomam o medicamento.2 O mecanismo deste efeito adverso não é completamente claro, mas especula-se que esteja relacionado com a quelação do cobre nas células da retina.4
A maioria dos pacientes com este efeito adverso tinha tomado doses de 60 a 100 mg/kg/dia com início dos sintomas após 2 a 12 meses de tratamento.4,29 A dose diária de etambutol aprovada pela FDA no tratamento da tuberculose é de 15 a 25 mg/kg/dia. Pensa-se que a neuropatia óptica induzida pelo etambutol está relacionada com a dose; ocorre a taxas de 18% dos doentes a uma dose de 35 mg/kg/dia, 5% a 6% a 25 mg/kg/dia, e menos de 1% a 15 mg/kg/dia.30 Recomenda-se o ajustamento da dose para doentes com insuficiência renal, uma vez que uma desobstrução inadequada do medicamento pode levar a uma toxicidade ocular adicional.
A perda de visão associada ao etambutol tem sido geralmente relatada como reversível; contudo, pode ser irreversível em certas populações, incluindo pacientes geriátricos e aqueles que receberam o medicamento cronicamente.30
Ethambutol está contra-indicado em pacientes com histórico de neurite óptica, a menos que o julgamento clínico justifique a sua utilização.31 Devem ser realizados exames oftalmológicos de base e periódicos; a informação prescrita para o etambutol recomenda exames mensais para pacientes que tomam >15 mg/kg/dia.31 Alguns autores sugeriram que os exames anuais podem ser apropriados para os pacientes que tomam <15 mg/kg/dia, com monitorização mais frequente para os pacientes com elevado risco de desenvolver neuropatia óptica. Isto incluiria doentes com mais de 60 anos ou menos de 16 anos; doentes com doença renal, alcoolismo, ou neuropatia periférica; doentes que tomam mais de 15 mg/kg/dia; ou tratamento por mais de 6 meses.2 Os doentes que apresentem sintomas de neuropatia óptica devem ser avaliados, e a droga deve ser descontinuada.
Isoniazida: Este antibiótico é outro fármaco utilizado no tratamento e prevenção da tuberculose. Tem sido relatado causar neuropatia óptica; contudo, uma vez que a isoniazida é utilizada em conjunto com o etambutol, que também está implicado na neuropatia óptica, determinar a causa dos problemas de visão é frequentemente difícil.20 Pensa-se que a neuropatia óptica induzida por isoniazida por isoniazida é menos frequente e reversível.2
Tratamento
A avaliação oftalmológica imediata é primordial, e que, juntamente com a descontinuação do fármaco ofensivo quando possível, constitui a base do tratamento da neuropatia óptica induzida por fármacos.4 Embora a descontinuação do fármaco seja frequentemente recomendada, isto pode nem sempre ser possível, uma vez que medicamentos como amiodarona, linezolida, e etambutol podem ser necessários para tratar o paciente de forma óptima. Nestas circunstâncias, é necessária uma monitorização cuidadosa e cuidados contínuos por um oftalmologista.
Implicações
Muitos medicamentos podem causar efeitos adversos oculares, e os riscos potenciais devem ser discutidos com os pacientes antes de iniciar a terapia. Os farmacêuticos estão na posição única de serem os prestadores de cuidados de saúde mais acessíveis; podem ser eles os pacientes que mais provavelmente consultarão quando sofrerem efeitos adversos devido aos seus medicamentos. Pode não ser possível conhecer todos os efeitos adversos oculares induzidos por medicamentos, mas é importante reconhecer que muitos medicamentos sistémicos podem afectar a saúde ocular. A detecção precoce pode potencialmente prevenir ou minimizar danos graves. Os farmacêuticos devem estar cientes de que a maioria dos pacientes que sofrem de neuropatia óptica induzida por fármacos apresentará uma diminuição da visão.2 Qualquer paciente que se queixe de um declínio súbito e indolor da visão deve ser aconselhado a comunicar imediatamente estas alterações.
Além de contactar a FDA e o fabricante do medicamento, os farmacêuticos podem comunicar casos suspeitos de neuropatia óptica induzida por fármacos ao Registo Nacional de Efeitos Oculares Induzidos por Medicamentos (www.eyedrugregistry.com). As informações que serão úteis na notificação de reacções adversas oculares incluem o nome, duração e dose do fármaco; tempo desde a ingestão do fármaco até ao início dos resultados; e quaisquer resultados de exames oftalmológicos.
1. O’Neill EC, Danesh-Meyer HV, Connell PP, et al. A cabeça do nervo óptico em neuropatias ópticas adquiridas. Nat Rev Neurol. 2010;6:221-236.
2. Lloyd MJ, Fraunfelder FW. Neuropatias ópticas induzidas por drogas. As drogas hoje em dia. 2007;43:827-836.
3. Spiteri MA, James DG. Reacções oculares adversas às drogas. Postgrad Med J. 1983;59:343-349.
4. Li J, Tripathi RC, Tripathi BJ. Perturbações oculares induzidas por drogas. Medicamentos seguros. 2008;21:127-141.
5. Kaakeh Y, Abel SR. Distúrbios visuais. In: Tisdale JE, Miller DA, eds. Doenças induzidas por drogas: Prevenção, Detecção, e Gestão. 2ª ed. Bethesda, MD: American Society of Health-Systems Pharmacists; 2010:
250-274.
6. Hatzimouratidis K, Hatzichristou D. Inibidores da fosfodiesterase tipo 5: no dia seguinte. Eur Urol. 2007;51:75-89.
7. Lee M. Capítulo 86. Disfunção eréctil. In: DiPiro JT, Talbert RL, Yee GC, et al, eds. Farmacoterapia: Uma Abordagem Fisiopatológica. 7ª ed., eds. Nova Iorque, NY: McGraw-Hill; 2010. www.accesspharmacy.com/content.aspx?aID=3209583. Acesso em 24 de Fevereiro de 2011.
8. Kerr NM, Danesh-Meyer HV. Inibidores da fosfodiesterase e do olho. Clin Experiment Ophthalmol. 2009;37:514-523.
9. Bischoff E. Potência, selectividade, e consequências da não-selectividade da inibição da PDE. Int J Impot Res. 2004;16(suppl 1):S11-S14.
10. Barbehenn E, Lurie P, Wolfe SM, et al. Petição à FDA para exigir um aviso de caixa negra para drogas de disfunção eréctil sildenafil (Viagra), tadalafil (Cialis), vardenafil (Levitra) para alertar para o potencial de perda irreversível da visão. Cidadão Público. 20 de Outubro de 2005. www.citizen.org/hrg1753. Acedido a 24 de Fevereiro de 2011.
11. Laties AM. Distúrbios da visão e inibidores da fosfodiesterase tipo 5: uma revisão das provas até à data. Segurança dos medicamentos. 2009;32:1-18.
12. Danesh-Meyer HV, Levin HA. Drogas de disfunção eréctil e risco de neuropatia óptica isquémica anterior: associação casual ou causal? Br J Ophthalmol. 2007;91:1551-1555.
13. Carter JE. Neuropatia óptica isquémica anterior e AVC com uso de inibidores de PDE-5 para disfunção eréctil: causa ou coincidência? J Neurol Sci. 2007;262:89-97.
14. Gorkin L, Hvidsten, Sobel RE, et al. Uso de citrato de Sildenafil e a incidência de neuropatia óptica isquémica anterior não artérica. Int J Clin Pract. 2006;60:500-503.
15. Pomeranz HD, Bhavsar AR. Neuropatia óptica isquémica não artérica que se desenvolve pouco depois da utilização de sildenafil (Viagra): um relatório de sete novos casos. J Neurol Ophthalmol. 2005;25:9-13.
16. Margo CE, DD francesa. Neuropatia isquémica óptica em veteranos masculinos prescreveu inibidores de fosfodiesterase 5. Am J Ophthalmol. 2007;143:538-539.
17. McGwin G, Vaphiades MS, Hall TA, et al. Neuropatia óptica isquémica anterior não artérica e o tratamento da disfunção eréctil. Br J Ophthalmol. 2006;90:154-157.
18. Fraunfelder FW. Efeitos secundários visuais associados aos agentes da disfunção eréctil. Am J Ophthalmol. 2005;140:723-724.
19. McKoy JM, Bolden CR, Samaras A, et al. Sildenafil- e tadalafil-associated optic neuropathy: implications for men after prostate cancer treatment. Comunidade Oncol. 2009;6:78-79.
20. Santaella RM, Fraunfelder FW. Efeitos adversos oculares associados a medicações sistémicas. Fármacos. 2007;67:75-93.
21. Johnson LN, Krohel GB, Thomas ER. O espectro clínico da neuropatia óptica associada à amiodarona-associada. J Nat Med Assoc. 2004;96:1477-1491.
22. Mantyjarvi M, Tuppurainen K, Ikaheimo K. Efeitos secundários oculares da amiodarona. Surv Ophthalmol. 1998;42:360-366.
23. Inserção da embalagem de Cordarone (amiodarona HCl). Filadélfia, PA: Wyeth Pharmaceuticals, Inc; Dezembro 2010.
24. Jahaveri M, Khurana RN, O’Hearn TM, et al. Neuropatia óptica induzida por Linezolida: uma desordem mitocondrial? Br J Ophthalmol. 2007;91:111-115.
25. Azamfirei L, Copotoiu SM, Branzaniuc K, et al. Cegueira completa após neuropatia óptica induzida por tratamento de curto prazo com linezolida num paciente que sofre de distrofia muscular. Pharmacoepidemiol Drug Saf. 2007;16:402-404.
26. Joshi L, Taylor SR, Large O, et al. Um caso de neuropatia óptica após utilização de linezolida a curto prazo num doente com leucemia linfocítica aguda. Dis. Clin Infect Dis. 2009;48:e73-e74.
27. Narita M, Tsuji BT, Yu VL. Neuropatia periférica e óptica associada à linezolida, acidose láctica, e síndrome da serotonina. Farmacoterapia. 2007;27:1189-1197.
28. Rucker JC, Hamilton SR, Bardenstein D, et al. Neuropatia óptica tóxica associada a linezolida. Neurologia. 2006;66:595-598.
29. Melamud A, Kosmorsky GS, Lee MS. Toxicidade ocular do etambutol. Mayo Clin Proc. 2003;78:1409-1411.
30. Kokkada SB, Barthakur R, Natarajan M, et al. Efeitos secundários oculares de drogas antituberculantes – um foco na prevenção, detecção precoce e gestão. Kathmandu Univ Med J. 2005;3:438-441.
31. Inserção da embalagem de Myambutol (ethambutol). Northport, NY: X-Gen Pharmaceuticals, Inc; Maio de 2007.
0 comentários