as fontes mais comuns do hidreto Nucleófilo são o hidreto de alumínio lítio (LiAlH4) e o boroidreto de sódio (NaBH4). Nota! O anião hidreto não está presente durante esta reacção; pelo contrário, estes reagentes servem como fonte de hidreto devido à presença de uma ligação metal-hidrogénio polar. Como o alumínio é menos electronegativo do que o boro, a ligação Al-H no LiAlH4 é mais polar, tornando assim o LiAlH4 um agente redutor mais forte.
Adição de um anião hidreto (H:-) a um aldeído ou cetona dá um anião alcóxido, que na protonação produz o álcool correspondente. Os aldeídos produzem 1º álcoois e as cetonas produzem 2º álcoois.
Em hidróxidos de metal, os sais de alcóxido resultantes são insolúveis e precisam de ser hidrolisados (com cuidado) antes que o produto alcoólico possa ser isolado. Na redução de borohidreto de sódio, o sistema de solvente metanol alcança esta hidrólise automaticamente. Na redução de hidreto de lítio de alumínio é normalmente adicionada água numa segunda etapa. O lítio, sódio, boro e alumínio acabam como sais inorgânicos solúveis no final de qualquer reacção. Nota! LiAlH4 e NaBH4 são ambos capazes de reduzir os aldeídos e as cetonas ao álcool correspondente.
Mecanismo
Este mecanismo é para uma redução LiAlH4. O mecanismo para uma redução de NaBH4 é o mesmo excepto que o metanol é a fonte de prótons utilizada na segunda etapa.
1) Ataque nucleófilo pelo anião hidreto
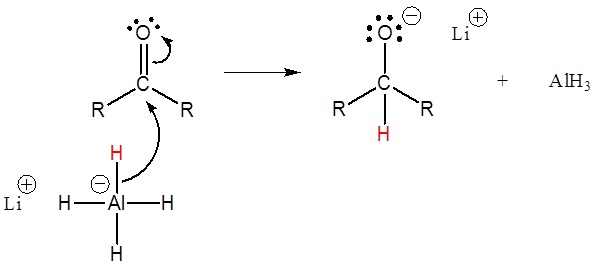
2) O alkoxide é protonado
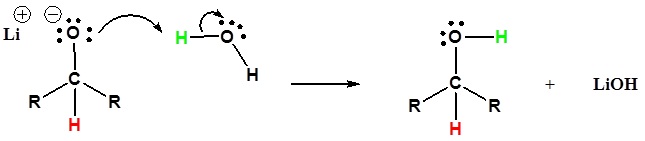
Passar de Reactantes a Produtos Simplificados
Propriedades de Fontes de Hidretos
Duas fontes práticas de hidretos…como reactividade são os complexos hidretos metálicos hidreto de lítio alumínio (LiAlH4) e borohidreto de sódio (NaBH4). Estes são ambos sólidos brancos (ou quase brancos), que são preparados a partir de hidretos de lítio ou de sódio por reacção com halogenetos de alumínio ou de boro e ésteres. O hidreto de lítio e alumínio é de longe o mais reactivo dos dois compostos, reagindo violentamente com água, álcoois e outros grupos ácidos com a evolução do gás hidrogénio. A tabela seguinte resume algumas características importantes destes reagentes úteis.
Seria óptimo converter esta tabela em texto.
Problemas
1) Por favor, desenhar os produtos das seguintes reacções:
2) Por favor, desenhar a estrutura da molécula que deve ser reagida para produzir o produto.
3) O óxido de deutério (D2O) é uma forma de água em que os hidrogénios foram substituídos por deutérios. Para a seguinte redução LiAlH4 a água tipicamente utilizada foi substituída por óxido de deutério. Por favor, desenhar o produto da reacção e colocar o deutério no local adequado. Dica! Veja o mecanismo da reacção.
Respostas
1)
2)
3)
Contribuidores
- Prof. Steven Farmer (Sonoma State University)
- William Reusch, Professor Emérito (Michigan State U.), Virtual Textbook of Organic Chemistry
0 comentários