John J. Chen, MD, PhD; Ryan M. Tarantola, MD; Christine N. Kay, MD; Vinit B. Mahajan, MD, PhD
Aggiornato da Jason P. Kam, MD,
in origine pubblicato: 30 agosto 2011
aggiornato: 14 settembre 2016
Denuncia principale: Luci vorticose e lampeggianti
Storia della malattia attuale
Una donna di 57 anni si è presentata alla clinica oftalmologica dell’UIHC lamentando fotopsie centrali bilaterali negli ultimi due anni. Soffriva di sindrome di Sjogren e artrite infiammatoria ed era attualmente trattata con prednisone e metotrexato. È stata precedentemente trattata con idrossiclorochina (Plaquenil) 200mg bid (6.5mg/kg) per 10 anni, che è stata interrotta un anno prima della presentazione: Nessuno
Anamnesi medica: Sindrome di Sjogren e artrite infiammatoria, tachicardia sopraventricolare, ansia, depressione, malattia dell’ulcera peptica
Medicazioni: prednisone, metotrexato, amitriptilina, ranitidina, estradiolo, tizanidina, diltiazem, Restasis
Allergies: codeina, droperidolo
Anamnesi familiare: malattie cardiache, artrite, cancro
Anamnesi sociale: alcol occasionale ma nessun uso di tabacco o droghe per via endovenosa.
Revisione dei sistemi:
Visione offuscata, aloni, occhio secco, bocca secca, reflusso gastroesofageo, dolore articolare
ESAME OCCULARE
Acutezza visiva
- Occhio destro (OD): 20/30
- Occhio sinistro (OS): 20/25
Pupille: Reattive alla luce in ogni occhio da 5 mm al buio a 2 mm alla luce. Nessun difetto pupillare afferente relativo (RAPD).
Movimenti extraoculari: Completi, entrambi gli occhi (OU)
Campi visivi a confronto: Pieno OU
Pressione intraoculare
- OD: 15 mmHg
- OS: 15 mmHg
Esterno
Esame con lampada a fessura
- Ciglia: normale
- Congiuntiva/Sclera: normale
- Cornea: chiara, senza verticillata
- Camera anteriore: profonda e tranquilla
- Iris: normale
- Lente: 1+ NS
- Vitreo: normale
Esame del fondo dilatato
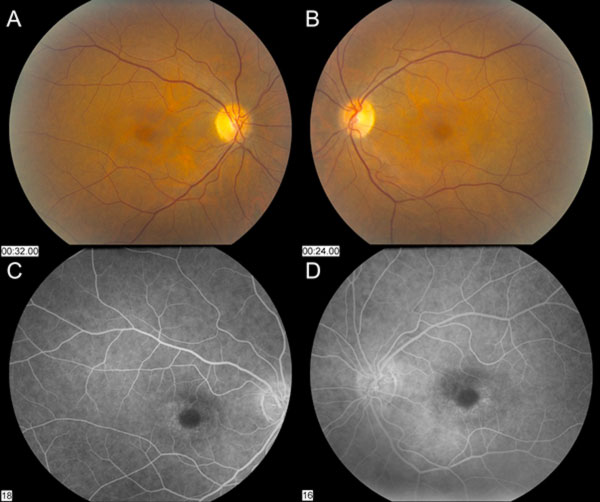
I nervi ottici sono apparsi sani con un rapporto tazza-disco di 0.3 di rapporto coppa-disco. C’era una lieve depigmentazione paracentrale del RPE nella macula che ha risparmiato la fovea centrale OU. I vasi e l’esame periferico erano normali OU (Figura 1). Non c’era alcun distacco posteriore del vitreo, lacerazioni retiniche o distacchi retinici.
Test accessori
Figura 1: Le foto del fundus dimostrano una lieve depigmentazione paracentrale del RPE che risparmia la fovea centrale in entrambi gli occhi destro (A) e sinistro (B). L’angiografia con fluoresceina mostra iperfluorescenza parafoveale OU (C e D).
Diagnosi: Tossicità retinica indotta dall’idrossiclorochina
La clorochina (CQ) e l’idrossiclorochina (Plaquenil) (HCQ) sono state usate per molti anni, inizialmente per il trattamento della malaria ma ora più comunemente per il trattamento di malattie infiammatorie come l’artrite reumatoide e il lupus . È ora considerato per nuove applicazioni di malattia nel diabete, nelle malattie cardiache e nelle terapie aggiuntive del cancro.
La clorochina e l’idrossiclorochina appartengono entrambe alla famiglia dei chinoloni e condividono indicazioni cliniche ed effetti collaterali simili, compresa la tossicità retinica. La tossicità retinica indotta dalla clorochina è stata descritta per la prima volta nel 1959 e gli effetti tossici retinici dell’idrossiclorochina sono stati descritti successivamente nel 1967. L’idrossiclorochina ha una tossicità retinica significativamente inferiore e ha ampiamente sostituito la clorochina come trattamento della malattia infiammatoria. Purtroppo, il danno retinico da questi farmaci è in gran parte irreversibile, quindi è fondamentale rilevare la tossicità retinica precoce nella speranza di limitare l’entità della perdita visiva.
Segno/Sintomi
Le manifestazioni oculari dell’idrossiclorochina includono verticillata corneale e tossicità retinica. I verticillati sono depositi corneali di sali all’interno dell’epitelio corneale. Questa condizione non causa sintomi ed è reversibile con la cessazione del farmaco. Il ritrovamento di verticillata corneali non ha alcuna correlazione con la tossicità retinica e non è un’indicazione a smettere il farmaco. Il segno distintivo della tossicità da idrossiclorochina è la retinopatia pigmentaria bilaterale. I pazienti con i primi risultati retinici sono spesso asintomatici pur avendo sottili scotomi paracentrali. Più tardi nella malattia, i pazienti possono sviluppare una maculopatia bilaterale dell’occhio di bue, caratterizzata da un anello di epitelio pigmentato retinico (RPE) depigmentato nella macula, risparmiando la fovea, che è spesso accompagnata da scotomi paracentrali e centrali. La tossicità da idrossiclorochina allo stadio finale porta ad una diffusa atrofia del RPE e della retina con una perdita della visione centrale, della visione periferica e della visione notturna. Studi recenti hanno dimostrato che i pazienti di origine asiatica sviluppano un danno iniziale in una distribuzione extramaculare più periferica vicino alle arcate, più frequentemente nella regione inferotemporale con corrispondenti difetti di campo superonasali. I pazienti afroamericani e ispanici mostrano un modello prevalentemente paravoveale simile ai soggetti europei.
I cambiamenti del fundus alla biomicroscopia, compresa la maculopatia dell’occhio di bue, sono indicativi di una tossicità retinica indotta dall’idrossiclorochina abbastanza avanzata che è in gran parte irreversibile nonostante la cessazione del farmaco. Il continuo deterioramento della funzione visiva può verificarsi dopo la sospensione dell’idrossiclorochina, probabilmente a causa della lenta eliminazione dalla retina e a livello sistemico. Lo screening è importante per rilevare la tossicità retinica precoce prima di cambiamenti funduscopici notevoli al fine di limitare la quantità di perdita visiva. La visione centrale può essere preservata se il danno viene riconosciuto prima che ci siano cambiamenti nell’epitelio pigmentato retinico (RPE).
Meccanismo
Il meccanismo di CQ e HCQ è poco conosciuto. Le molecole si legano alla melanina del RPE causando cambiamenti metabolici ed effetti tossici. I depositi colpiscono la retina esterna, lo strato dei fotorecettori e il RPE, ma preservano la retina interna.
Prevalenza
Anche se la tossicità retinica da idrossiclorochina è ritenuta rara, studi recenti suggeriscono che potrebbe avere una prevalenza maggiore di quella precedentemente riconosciuta. Un grande studio che ha esaminato pazienti con più di 5 anni di uso di HCQ sono stati valutati con campi visivi 10-2 o tomografia a coerenza ottica a dominio spettrale (SD OCT). La prevalenza complessiva di tossicità in questo gruppo era del 7,5% con un’ampia variazione nella dose giornaliera e nella durata d’uso. Oltre questo punto il rischio aumenta bruscamente al 20% dopo 20 anni. Il rischio è più basso con una dose più bassa, tuttavia non c’è un vero dosaggio sicuro per una lunga durata d’uso.
Un altro studio su 4000 pazienti ha trovato una prevalenza di 6,8/1000 pazienti. I fattori di rischio che aumentano la possibilità di retinopatia da idrossiclorochina includono la dose giornaliera, la dose cumulativa, la malattia renale o epatica, l’età e la precedente malattia retinica. Una dose giornaliera di > 6,5mg/kg (peso corporeo ideale) pone i pazienti a maggior rischio, ma una dose giornaliera inferiore a questo livello non ha precluso al paziente di sviluppare tossicità dopo molti anni di trattamento. Una dose cumulativa di >1000g di idrossiclorochina o 460g di clorochina era probabilmente il fattore di rischio maggiore, che è stato tipicamente raggiunto dopo 5-7 anni di un dosaggio tipico . Tuttavia, ci sono stati casi di pazienti con tossicità da idrossiclorochina già dopo 1,9 mesi dall’inizio del trattamento.
| Dose giornaliera | |
|
HCQ |
>5.0 mg/kg di peso reale |
|
CQ |
>2.3 mg/kg di peso reale |
|
Durata d’uso |
>5 anni; nessun altro fattore di rischio |
|
Malattia renale |
Riduzione della velocità di filtrazione glomerulare (GFR) |
|
Farmaci concomitanti |
Uso di Tamoxifene |
|
Malattia maculare |
Maggiore suscettibilità alla tossicità |
|
Età |
Nessuna associazione significativa tra età e rischio di tossicità |
|
Malattia epatica |
Nessuna chiara associazione tra malattia epatica e tossicità |
|
Genetica |
Nessuna chiara associazione con fattori genetici e tossicità |
Il rischio più critico per la tossicità è l’eccessiva dose giornaliera per peso. Il dosaggio > 5.0mg/kg aumenta il rischio di tossicità. La durata d’uso è anche un fattore di rischio critico. Le raccomandazioni precedenti nel 2011 notavano che la dose cumulativa (dose giornaliera x durata in anni) era un indicatore di rischio, tuttavia la valutazione più accurata è sulla base della durata d’uso relativa alla dose giornaliera per peso reale come si vede nella figura qui sotto. Un altro cambiamento rispetto alle raccomandazioni del 2011 è stato che il peso reale era meglio del peso ideale per il calcolo della dose e il rischio più basso è stato raggiunto con dosi di 5 mg/kg di peso reale.
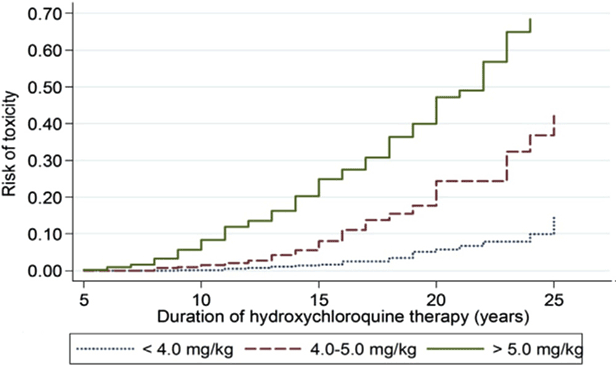
Figura 6: Questa è una curva di Kaplan Meier che mostra il rischio cumulativo di retinopatia nel tempo, con diversi livelli di uso di idrossiclorochina (HCQ). Quando l’uso è tra 4.0 e 5.0 mg/kg, il rischio è molto basso entro i primi 5 a 10 anni, ma aumenta notevolmente in seguito. Riprodotto da Melles e Marmor, 2014
L’HCQ viene eliminato dai reni e quindi la malattia renale aumenta il rischio di tossicità. Pertanto, sia il dosaggio che la frequenza dello screening possono dover essere regolati. L’uso del tamoxifene (usato nel trattamento del cancro al seno) aumenta il rischio di tossicità di circa 5 volte). Il meccanismo di questo collegamento non è compreso. I pazienti con malattia retinica sottostante possono essere a più alto rischio di tossicità, ma nessun dato specifico lo ha confermato. Tuttavia, la maculopatia rende l’implementazione e l’interpretazione dello screening più difficile.
Linee guida per lo screening
L’American Academy of Ophthalmology (AAO) ha recentemente fornito raccomandazioni riviste per lo screening che incorporano i nuovi progressi della tecnologia che permettono di individuare più presto la malattia nel 2016.
|
Tempistica |
Test accessori |
|
|---|---|---|
|
Screening di base |
Entro il primo anno di utilizzo |
Campi visivi e SD OCT se è presente una maculopatia |
|
Schermo annuale |
Iniziare dopo 5 anni di utilizzo ma prima se presenza di fattori di rischio importanti |
Entrambi HVF 10-2 e SD-OCT; test opzionali (secondo necessità): mfERG e/o FAF |
Esame di base: Tutti i pazienti devono essere sottoposti a un esame oftalmologico di base entro il primo anno dall’inizio della terapia con HCQ o CQ con un’accurata valutazione dei fattori di rischio e un esame del fondo della macula per escludere una malattia sottostante. Il campo visivo basale e la SD OCT sono raccomandati se sono presenti anomalie (per esempio lesioni maculari, glaucoma, ecc.) che potrebbero influenzare i test di screening.
Screening annuale: Il rischio di tossicità è raro nei primi anni di trattamento con HCQ e CQ. In assenza di fattori di rischio importanti, lo screening può essere rimandato per 5 anni. La tossicità si sviluppa lentamente e un esame annuale dopo il 5° anno è sufficiente. Uno screening più precoce è raccomandato per i pazienti con uno qualsiasi dei fattori di rischio menzionati in precedenza. Gli esami di screening annuali comprendono la biomicroscopia, il campo visivo automatizzato 10-2 e la tomografia a coerenza ottica nel dominio spettrale (SD-OCT) con autofluorescenza del fondo (FAF) e/o elettroretinogramma multifocale (mfERG) opzionale, secondo necessità.
Il campo visivo Humphrey 10-2 è sensibile al rilevamento di sottili difetti del campo visivo paracentrale ed è raccomandato durante tutte le visite di screening. Il test SITA con tracciati di deviazione del modello è raccomandato. Modelli di test più ampi 24-2 o 30-2 sono necessari per i pazienti asiatici a causa della possibilità di manifestazioni extra-maculari di tossicità. Gli schemi di test grandi testano solo 4 punti centralmente. Nelle linee guida dell’AAO per i pazienti asiatici non si parla di testare sia il 10-2 che i modelli di test grandi.
SD-OCT: A differenza della tomografia a coerenza ottica nel dominio del tempo, SD-OCT ha la risoluzione per rilevare un assottigliamento localizzato della retina nella regione parafoveale. Su SD-OCT, la perdita o l’assottigliamento dello strato parafoveale e perifoveale dei fotorecettori e la rottura focale delle laminazioni del segmento esterno sono coerenti con la tossicità. Questi cambiamenti sulla SD-OCT possono essere visti prima che siano presenti anomalie funduscopiche. Le scansioni ad angolo più ampio o le scansioni attraverso le arcate vascolari sono importanti per gli occhi asiatici.
Altri test utili
Elettroretinogramma multifocale (mf-ERG): Questo test permette di rilevare una depressione parafoveale o extramaculare localizzata nella retinopatia iniziale. Questo ha una sensibilità simile ai campi visivi e può fornire una conferma oggettiva della sospetta perdita di campo paracentrale.
Autofluorescenza del fondo (FAF): La tossicità precoce dell’idrossiclorochina può anche essere rilevata all’autofluorescenza come un aumento dell’anello di segnale nelle regioni parafoveale ed extramaculare, che è indicativo della disfunzione dei fotorecettori e del RPE. La malattia più avanzata porterà alla perdita di autofluorescenza in queste regioni a causa della perdita di fotorecettori e RPE, spesso con iperfluorescenza circostante.
Test non raccomandati: Recenti linee guida sconsigliano la sola biomicroscopia, la fotografia del fundus, la tomografia a coerenza ottica nel dominio del tempo, l’angiografia con fluoresceina, l’elettroretinogramma a pieno campo, la griglia di Amsler, il test della visione a colori e l’elettro-oculogramma. Si pensa che tutti questi test abbiano una sensibilità inadeguata per rilevare la tossicità dell’HCQ/CQ in una fase abbastanza precoce da prevenire una significativa perdita della vista.
In sintesi, la tossicità retinica indotta dall’idrossiclorochina è probabilmente più diffusa di quanto si credesse in precedenza. Una volta si pensava che fosse sicuro ad una dose giornaliera di < 6.5mg/kg/giorno, studi più recenti mostrano che molti anni di trattamento con idrossiclorochina ad una “dose sicura” possono ancora portare a tossicità. Linee guida più recenti affermano che la dose giornaliera >5mg/kg di peso reale/giorno può portare alla tossicità. La tossicità retinica è irreversibile e può progredire dopo la cessazione dell’idrossiclorochina, quindi lo screening precoce è importante per limitare la potenziale perdita della vista. Si raccomanda uno screening di base e uno screening annuale dopo cinque anni. Modalità di test ancillari, come SD-OCT, mfERG e autofluorescenza forniscono strumenti di screening sensibili che completano la HVF 10-2 nel rilevamento della tossicità precoce dell’idrossiclorochina.
Storia clinica completa e decorso
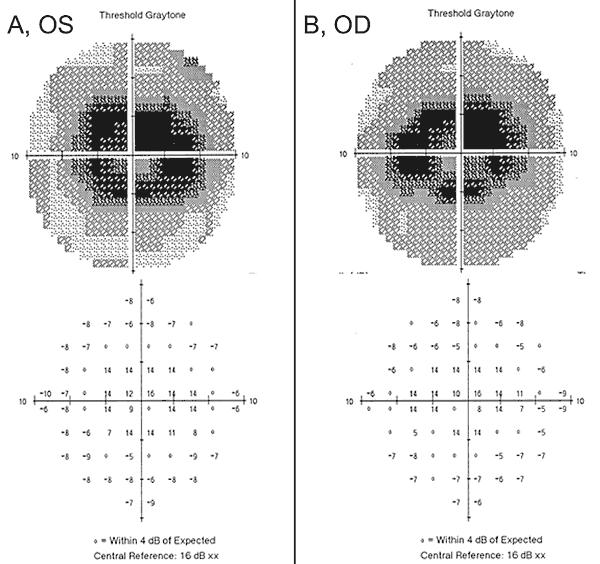
Il nostro paziente evidenzia alcuni dei nuovi risultati nella tossicità retinica da idrossiclorochina, compresa l’importanza dello screening precoce con gli strumenti appropriati descritti sopra, la mancanza di sensibilità di alcuni dei test obsoleti e il potenziale di peggioramento nonostante la cessazione del farmaco incriminato. Quando la nostra paziente si è presentata inizialmente con aloni e luce vorticosa a un fornitore esterno, aveva un’acuità visiva normale e nessun difetto sulla griglia di Amsler, sul test della visione a colori o sull’esame del fondo dilatato. Inoltre, il suo 24-2 HVF un anno prima ha dimostrato cambiamenti paracentrali non specifici ed è stato considerato completo. Un anno dopo, è stato ottenuto un 10-2 HVF che ha mostrato densi scotomi paracentrali bilateralmente (Figura 2), nonostante la normale acuità visiva, griglia Amsler e test di visione a colori. Al rilevamento dei difetti del campo visivo, l’idrossiclorochina è stata interrotta. Stava prendendo l’idrossiclorochina > 5.0 mg/kg/die per una durata di 10 anni con una dose cumulativa di 1460g che la metteva a maggior rischio di tossicità retinica da idrossiclorochina.
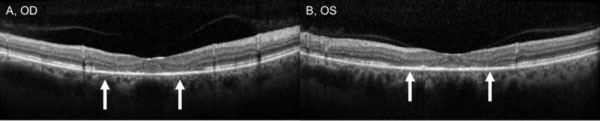
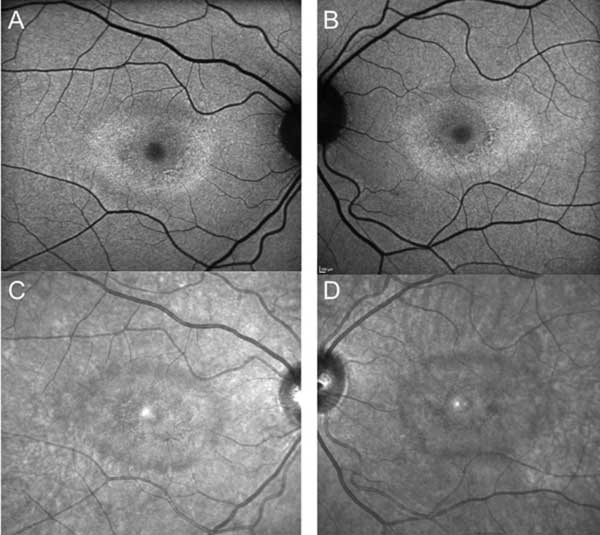
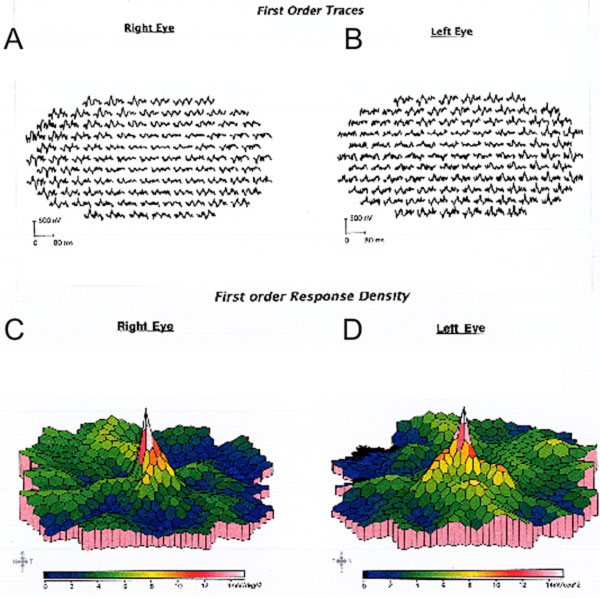
Nonostante la cessazione dell’idrossiclorochina, un anno di follow-up ha rivelato un lieve peggioramento dell’acuità visiva a 20/30 OD e 20/25 OS, con nuove anomalie sulla griglia di Amsler e deficit al test della visione a colori. Sottile depigmentazione parafoveale RPE potrebbe essere visto su biomicroscopia, che è stato evidenziato da iperfluorescenza su angiografia fluoresceina (Figura 1). La ripetizione del test HVF 10-2 ha dimostrato i densi scotomi paracentrali. SD-OCT ha mostrato la perdita della giunzione parafoveale segmento interno/esterno, assottigliamento dello strato nucleare esterno parafoveale, e una perdita della normale depressione foveale, che è caratteristica per la tossicità retinica idrossiclorochina (Figura 3). L’imaging di autofluorescenza ha mostrato un anello di iper-autofluorescenza nella regione parafoveale corrispondente al danno dei fotorecettori e alla disfunzione del RPE (Figura 4). Il MfERG ha dimostrato un segnale diminuito centralmente in entrambi gli occhi (Figura 5). Il nostro paziente dimostra l’importanza di utilizzare i nuovi strumenti di screening raccomandati per il rilevamento della tossicità precoce dell’idrossiclorochina. 10-2 HVF, SD-OCT, autofluorescenza o mfERG avrebbero potuto rilevare la tossicità retinica da idrossiclorochina il giorno della presentazione dei sintomi e possibilmente prima, limitando potenzialmente la quantità di perdita visiva.
Diagnosi differenziale
- degenerazione maculare legata all’età
- distrofia coroideale areolare centrale
- malattia di Stargardt
- cone-distrofia delle aste
- distrofia anulare concentrica benigna
SCREENING CONSIGLIATO
Screening annuale precoce per pazienti che hanno fattori di rischio per sviluppare tossicità da idrossiclorochina. |
Segni
Fattori di rischio:
|
SINTOMI
|
Trattamento
|
- Tehrani R, Ostrowski RA, Hariman R, Jay WM: tossicità oculare di idrossiclorochina. Semin Ophthalmol 2008, 23(3):201-209.
- Marmor MF, Kellner U, Lai TY, Lyons JS, Melles RB, Mieler WF: Recommendations on screening for chloroquine and hydroxychloroquine retinopathy (2016 Revision). Ophthalmology 2016, 123:1386-1394.
- Hobbs HE, Sorsby A, Freedman A: Retinopathy following chloroquine therapy. Lancet 1959, 2(7101):478-480.
- Shearer RV, Dubois EL: Ocular changes induced by long-term hydroxychloroquine (plaquenil) therapy. Am J Ophthalmol 1967, 64(2):245-252.
- Gass JDM: Stereoscopic atlas of macular diseases: diagnosis and treatment, 4th edn. St. Louis: Mosby; 1997.
- Melles RB, Marmor MF. Retinopatia pericentrale e differenze razziali nella tossicità da idrossiclorochina. Oftalmologia 2015;122:110-6.
- Melles RB, Marmor MF. Il rischio di retinopatia tossica nei pazienti in terapia a lungo termine con idrossiclorochina. JAMA Ophthalmol 2014;132:1453-60.
- Wolfe F, Marmor MF: Rates and predictors of hydroxychloroquine retinal toxicity in patients with rheumatoid arthritis and systemic lupus erythematosus. Arthritis Care Res (Hoboken) 2010, 62(6):775-784.
- Marmor MF, Kellner U, Lai TY, Lyons JS, Mieler WF: Revised recommendations on screening for chloroquine and hydroxychloroquine retinopathy. Ophthalmology 2011, 118(2):415-422.
- Lyons JS, Severns ML: Detection of early hydroxychloroquine retinal toxicity enhanced by ring ratio analysis of multifocal electroretinography. Am J Ophthalmol 2007, 143(5):801-809.
- Yam JC, Kwok AK: Ocular toxicity of hydroxychloroquine. Hong Kong Med J 2006, 12(4):294-304.
- Michaelides M, Stover NB, Francis PJ, Weleber RG: Retinal toxicity associated with hydroxychloroquine and chloroquine: risk factors, screening, and progression despite cessation of therapy. Arch Ophthalmol 2011, 129(1):30-39.
- Chen E, Brown DM, Benz MS, Fish RH, Wong TP, Kim RY, Major JC: Spectral domain optical coherence tomography as an effective screening test for hydroxychloroquine retinopathy (the “flying saucer” sign). Clin Ophthalmol 2010, 4:1151-1158.
- Kellner U, Renner AB, Tillack H: Fundus autofluorescence and mfERG for early detection of retinal alterations in patients using chloroquine/hydroxychloroquine. Invest Ophthalmol Vis Sci 2006, 47(8):3531-3538.
- Lai TY, Chan WM, Li H, Lai RY, Lam DS: Multifocal electroretinographic changes in patients receiving hydroxychloroquine therapy. Am J Ophthalmol 2005, 140(5):794-807.
- Bernstein HN: Ocular safety of hydroxychloroquine. Ann Ophthalmol 1991, 23(8):292-296.
Formato di citazione suggerito:
Kam JP. Revisione di EyeRounds.org. September 14, 2016; Available from: http://EyeRounds.org/cases/139-plaquenil-toxicity.htm.
0 commenti