I pazienti che hanno una malattia che richiede la cooperazione di medici di diverse specialità affrontano rischi a causa della cattiva comunicazione, dei diversi obiettivi percepiti e delle basi di conoscenza variabili tra le sottospecialità. Un esempio riguarda la prescrizione di idrossiclorochina da parte degli internisti per le malattie autoimmuni e lo screening per il dosaggio tossico e la retinopatia da parte degli oftalmologi. In questa panoramica, identificherò le lacune nella comprensione e nella comunicazione tra le specialità che portano a casi evitabili di retinopatia, e discuterò come è possibile colmarle.
Un problema persistente
Perché continuano a svilupparsi casi di retinopatia da idrossiclorochina, quando la sua patogenesi è nota dagli anni ’80? Tra le varie cause che contribuiscono, la principale è che a troppi pazienti vengono prescritte dosi giornaliere tossiche.1 L’idrossiclorochina viene immagazzinata nei tessuti magri, ed è largamente esclusa dal grasso.2 Pertanto, il dosaggio dell’HC dovrebbe essere basato sulla massa corporea magra.3 Nella maggior parte delle persone questo può essere determinato dalle tabelle del peso corporeo ideale (IBW) basate sull’altezza. Tuttavia, nei pazienti magri e astenici in cui il peso corporeo effettivo è inferiore a quello ideale, il dosaggio dovrebbe essere basato sul peso corporeo effettivo (ABW), non sull’IBW.4 Sebbene esistano alcuni casi, è estremamente raro sviluppare HR se la dose giornaliera non supera i 6,5 mg/kg basati sull’utilizzo del minore tra ABW e IBW per il denominatore.5
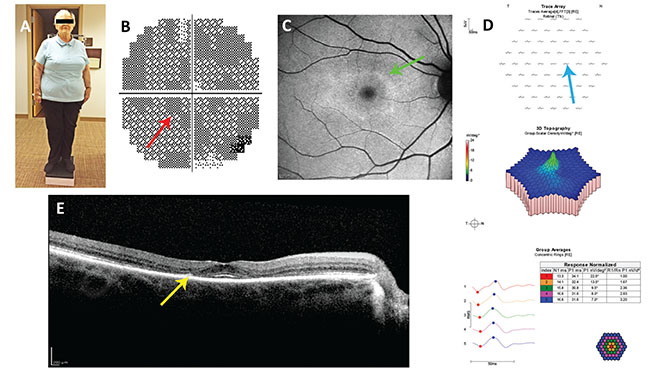
Figura 1. Caso di studio #1. A: Si noti il somatotipo. Nel paziente basso e obeso, il dosaggio basato sul peso corporeo ideale, non sul peso corporeo effettivo, è appropriato. B: Scotomata paracentrale (freccia rossa) nel suo test del campo visivo 10-2 del 2012, mancato dal suo oculista. C: Anulus of hyperautofluorescence (freccia verde) sull’imaging di autofluorescenza del fundus blu del 2014. D: Ampiezze d’onda paracentrali ridotte (freccia blu) sull’elettroretinografia multifocale. E: perdita paracentrale della linea ellissoidale e assottigliamento dello strato nucleare esterno (freccia gialla) sulla tomografia a coerenza ottica nel dominio spettrale.
Le pubblicazioni oftalmiche sono parzialmente responsabili della confusione che esiste riguardo all’importanza del dosaggio giornaliero nella prevenzione dell’HR. Considerate cosa dicono tre serie consecutive di linee guida dell’American Academy of Ophthalmology (tabella 1): Le linee guida del 2002 affermano che la dose giornaliera è di “fondamentale importanza” e consigliano l’uso dell’ABW tranne che nei pazienti obesi, nel qual caso si raccomanda l’IBW. Nel 2011, le linee guida si sono capovolte, scontando l’importanza della dose giornaliera a meno che un paziente sia obeso, nel qual caso si consiglia il dosaggio di IBW. Nel 2016, le linee guida si sono ribaltate, riaffermando l’importanza della dose giornaliera, ma scontando il dosaggio da IBW mentre sottolineano il dosaggio da ABW e introducendo un diverso fattore di conversione.
Con tale incoerenza, è facile capire come reumatologi e oftalmologi potrebbero essere confusi circa l’importanza della dose giornaliera e come dovrebbe essere calcolato. Le linee guida del 2002 erano potenzialmente pericolose a causa della loro mancanza di specificità su come usare ABW o IBW nel calcolo della dose giornaliera. Le linee guida del 2011 erano potenzialmente pericolose per la persona il cui ABW è inferiore all’IBW (vedi caso 1). Le linee guida del 2016 sono pericolose per la persona obesa in cui l’IBW è inferiore all’ABW (Vedi caso 2).
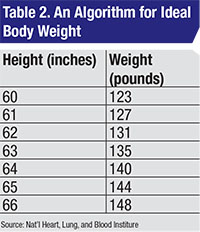
La prescrizione sicura dell’idrossiclorochina non è difficile. Si prende il minore tra ABW e IBW in base all’altezza.4 La dose giornaliera non dovrebbe superare i 6,5 mg/kg/d in base al minore tra ABW e IBW. Quale algoritmo usare per l’IBW è controverso, ma come preoccupazione pratica, probabilmente non ha importanza. Io preferisco l’algoritmo del National Heart, Lung, and Blood Institute (Tabella 2).3
Nelle sezioni seguenti, descriverò i casi di studio che coinvolgono l’HC e spiegherò i problemi di dosaggio coinvolti.
Caso #1
Una donna di 74 anni con artrite reumatoide è stata iniziata con idrossiclorochina 400 mg/d nel 2004. Era alta 1,5 m, pesava 198 libbre e non aveva insufficienza renale o epatica (Figura 1). È stata indirizzata per la prima volta dal suo reumatologo per lo screening della retinopatia nel 2012, e aveva perso l’occhio sinistro a causa di un trauma da bambino.
L’oculista che l’ha visitata nel 2012 le ha trovato un’acuità visiva corretta di 20/20 nell’occhio destro e ha interpretato il suo campo visivo 10-2 e l’elettroretinogramma multifocale come normali, sebbene non lo fossero. Non ha riconosciuto il suo dosaggio tossico e non ha fatto alcuna raccomandazione per cambiarlo. Le fu chiesto di tornare tra sei mesi, ma non lo fece mai.
Un altro oftalmologo la visitò nel 2014. La sua acuità visiva corretta era di 20/20 nell’occhio destro e il suo esame del fondo era normale. Una VF 10-2 con un oggetto rosso ha mostrato la progressione di uno scotoma anulare che era presente nel 2012. Uno studio di tomografia a coerenza ottica nel dominio spettrale della macula ha mostrato la perdita della zona ellissoide parafoveale e l’assottigliamento dello strato nucleare esterno.
Questo caso illustra le seguenti trappole evitabili, comunemente viste nella gestione multidisciplinare del paziente che prende HC:
– Il reumatologo ha prescritto una dose tossica di HC basata sull’altezza e sul peso del paziente. Il paziente era alto un metro e mezzo, con un peso corporeo ideale di 123 libbre (55,9 kg, vedi tabella 2) e una dose massima giornaliera sicura di 55,9 x 6,5 = 363 mg/d di HC. Per raggiungere questo risultato utilizzando la dimensione disponibile della pillola di 200 mg, si considera il fatto che l’HC ha una lunga emivita (circa 40 giorni1). Così, si può omettere un giorno di dosaggio in una settimana e arrivare a una dose media giornaliera adeguata. In una settimana, questa paziente può assumere fino a 7 x 363=2.543 mg di HC in modo sicuro. Se prende due compresse al giorno dal lunedì al sabato e salta l’HC la domenica, la sua dose settimanale totale sarà di 2.400 mg che equivale a una media di 2.400/7=343 mg/d, che è meno di una dose tossica.
– La paziente non ha avuto alcun esame di screening oftalmico di base e non è stata inviata per lo screening da un oftalmologo fino a otto anni di terapia. Questo è avvenuto nonostante la paziente avesse un alto rischio di tossicità basato sul suo dosaggio giornaliero. Le linee guida dell’AAO affermano che un esame di base dovrebbe essere ottenuto e poi, per i pazienti a basso rischio, gli esami annuali dovrebbero iniziare cinque anni dopo. Gli oftalmologi hanno regolarmente respinto queste raccomandazioni.4,7 Piuttosto che continuare a raccomandare una lacuna nello screening che è respinta da coloro che hanno il compito di controllare la retinopatia, sarebbe meglio se le linee guida abbracciassero la realtà pratica che lo screening annuale è la norma, che nei primi anni è principalmente finalizzata a rilevare e correggere il dosaggio giornaliero tossico.
– Il medico non è riuscito a riconoscere e correggere il dosaggio tossico di HC. Il dosaggio tossico è costantemente riscontrato nel 12,8-74,7% dei pazienti che assumono HC.4,8-10 Correggere il dosaggio giornaliero tossico è l’azione più comune intrapresa dall’oftalmologo dello screening, ed è la ragione principale per sottoporre a screening i pazienti che assumono HC. Quando si presume un dosaggio sicuro, come in Gran Bretagna, lo screening non è raccomandato perché la rarità dell’HR in queste circostanze lo rende uno spreco di risorse scarse.11
– Il primo oftalmologo non ha riconosciuto l’evidenza di tossicità sulla VF iniziale 10-2. La diagnosi di HR si basa su test ausiliari: 10-2 VF; SD-OCT; mfERG; e fundus autofluorescence imaging. Gli oftalmologi che effettuano lo screening per l’HR hanno l’obbligo di capire cosa costituisce un test positivo, quali sono i potenziali artefatti e come utilizzare modalità multiple per aumentare la fiducia clinica in una diagnosi. L’argomento è stato esplorato a fondo in diverse pubblicazioni.1,12,13 L’incapacità di interpretare correttamente i test del paziente ha costituito la base di grandi risarcimenti per malpractice in casi mancati di HR.
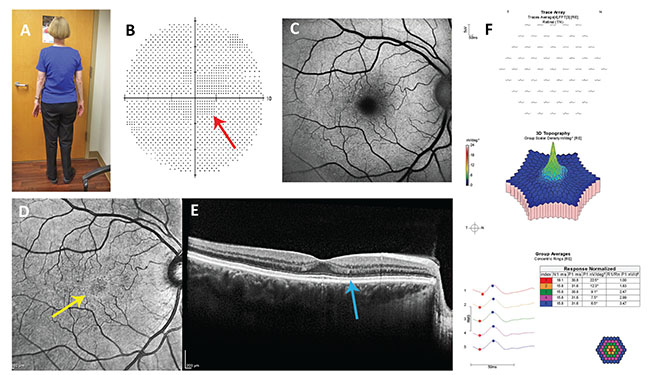
Figura 2. Case report #2: A: Si noti il somatotipo. Nel paziente astenico, il dosaggio basato sul peso corporeo effettivo, non sul peso corporeo ideale, è appropriato. B: Lo scotoma centrale non riproducibile (freccia rossa) nel suo test del campo visivo 10-2 non è tipico della retinopatia da idrossiclorochina. C: L’autofluorescenza del fundus blu è normale. D: La riflettanza nel vicino infrarosso mostra un anello iperriflettente (freccia gialla) che ha bassa sensibilità e specificità per la retinopatia da idrossiclorochina. E: La riflettività della linea ellissoidale nella parafovea è leggermente inferiore a quella della fovea, un segno potenzialmente precoce di retinopatia. F: L’elettroretinografia multifocale è normale.
Case Report #2
Nel 2015, un oftalmologo ha esaminato una donna di 63 anni con artrite reumatoide che aveva assunto HC 400 mg/d dal 1990 (25 anni, 3.650 g di dose cumulativa). Era alta 5 piedi e 3 pollici e pesava 112 libbre. Non aveva malattie renali o epatiche. La sua acuità visiva corretta era di 20/20 e il suo esame del fondo era normale bilateralmente. Il suo campo visivo 10-2 eseguito con un oggetto rosso ha mostrato uno scotoma centrale relativo non riproducibile (Figura 2). Il suo fundus autofluorescence imaging era normale. L’imaging di riflettanza nel vicino infrarosso ha mostrato un debole anello iperriflettente, che è stato inconsistentemente associato a HR precoce.14 La SD-OCT ha mostrato una linea ellissoidale leggermente meno iperriflettente e un suggerimento di assottigliamento dello strato nucleare esterno. L’elettroretinografia multifocale era normale.
Perché non c’era una retinopatia definita, è stata autorizzata a continuare l’uso di HC, ma il suo dosaggio tossico è stato corretto. Il minore tra il suo ABW e IBW era il suo ABW, che era di 112 libbre. Pertanto, il limite superiore della sua dose giornaliera sicura era di 330 mg. Le è stato raccomandato di non assumere più di 200 mg/d per i prossimi sei mesi, durante i quali è stato raccomandato di ripetere i test accessori per determinare se ci fosse un segnale di retinopatia precoce, data la sua grande dose cumulativa.
Anche le pubblicazioni reumatologiche contribuiscono alla confusione sul dosaggio. In un articolo online di aprile del sito web di reumatologia RheumNow.com, l’autore scrive: “I fattori di rischio noti per lo sviluppo di depositi oculari includono la durata della terapia, la dose cumulativa e la funzione renale”.15 Non menziona il fattore di rischio più importante, e l’unico modificabile, il dosaggio giornaliero. Continua scrivendo: “L’American Academy of Ophthalmology (AAO) consiglia un dosaggio basato sul peso di 6,5 mg/kg, con un limite massimo di 400 mg/giorno. Fanno eccezione gli individui di bassa statura e i pazienti obesi, per i quali l’AAO consiglia di calcolare il dosaggio in base al peso corporeo ideale per l’altezza”. Questo però non è ciò che afferma il riferimento citato. Invece, afferma: “La raccomandazione precedente enfatizzava il dosaggio in base al peso. Tuttavia, alla maggior parte dei pazienti vengono abitualmente somministrati 400 mg di HCQ al giorno… Questa dose è ora considerata accettabile, ad eccezione degli individui di bassa statura, per i quali la dose dovrebbe essere determinata sulla base del peso corporeo ideale per evitare il sovradosaggio. “16
L’autore continua, “La sensibilità e la specificità di questi test non sono ancora note per la tossicità retinica legata all’idrossiclorochina. C’è un alto tasso di anomalie di base, in particolare in coloro che sono anziani o hanno una malattia comorbida, che rendono i cambiamenti difficili da interpretare. Un altro problema è che il lupus eritematoso sistemico stesso si associa alla presenza di anomalie retiniche, aggiungendo ulteriore complessità alla decifrazione di questi test”. Queste sono affermazioni errate. La sensibilità relativa e la specificità dei test sono note (il mfERG è il più sensibile, il 10-2 VF il successivo, e lo SD-OCT il minore; lo SD-OCT è il più specifico, il 10-2 VF il successivo, e lo mfERG il minore).17 Il tasso di anomalie di base è alto per il test 10-2 VF, ma non per lo SD-OCT o lo mfERG. Il LES raramente influenza nessuno dei test.

Infine, l’autore raccomanda un dosaggio basato su 6,5 mg/kg/peso corporeo effettivo. Questa è una raccomandazione pericolosa per il paziente basso e obeso, come esemplificato nel Case Report 1.
In una revisione reumatologica di HR gli autori hanno scritto: “Uno studio francese ha dimostrato che la concentrazione di HC nel sangue intero >1.000 ng/ml ha ridotto il rischio di riacutizzazioni del lupus. La misurazione dei livelli ematici di HC può suggerire che alcuni pazienti richiedono >6,5 mg/kg/giorno per raggiungere il livello raccomandato. Questi pazienti non dovrebbero essere a maggior rischio di tossicità, purché i livelli siano monitorati, ma può essere importante monitorare anche la dose cumulativa quando si valuta il rischio di tossicità oculare. “18 La dichiarazione suggerisce erroneamente che esiste una relazione nota tra i livelli ematici di HC e l’HR, ma questo non è il caso.
Se gli internisti prescrittori e gli oftalmologi di screening mettessero in pratica una comprensione più chiara del corretto dosaggio giornaliero, la prevalenza di HR diminuirebbe. Nella maggior parte dei casi, la condizione è iatrogena e può essere evitata. Il dosaggio giornaliero è l’unico fattore di rischio modificabile e merita la massima attenzione nelle visite di screening, soprattutto nei primi cinque anni di utilizzo del farmaco, prima che il carico irreversibile e cumulativo si sia accumulato e aumenti il rischio di retinopatia. La raccomandazione che i casi a basso rischio abbiano omesso lo screening per cinque anni dopo un esame di base è stata ampiamente respinta da coloro che fanno lo screening, ed è probabilmente fuorviante data l’alta prevalenza del dosaggio tossico. Il rilevamento e la correzione del dosaggio tossico è di maggior valore per la prevenzione della retinopatia nei primi anni di assunzione di HC. I casi estremamente rari che sviluppano la retinopatia nonostante il dosaggio sicuro hanno più probabilità di essere rilevati quando un test ausiliario più sensibile e più specifico, per esempio, 10-2 VF e SD-OCT, sono usati insieme e quando l’interpretazione è fatta con competenza.
Il dottor Browning è uno specialista della retina presso Charlotte Eye, Ear, Nose, and Throat Associates. Contatta il dottor Browning al 6035 Fairview Rd, Charlotte, NC 28210. Può essere raggiunto al (704)-295-3180, o [email protected].
1. Browning DJ. Idrossiclorochina e retinopatia da clorochina. New York: Springer, 2014.
2. McChesney EW, Banks WF Jr, Fabian RJ. Distribuzione tissutale di clorochina, idrossiclorochina e desetilclorochina nel ratto. Toxic App Pharm 1967;10:501-513.
3. Browning DJ, Lee C, Rotberg D. L’impatto di diversi algoritmi per il peso corporeo ideale sullo screening della retinopatia da idrossiclorochina nelle donne. Clinical Ophthalmology 2014;8:1401.
4. Browning DJ. Impatto della revisione delle linee guida dell’American Academy of Ophthalmology per quanto riguarda lo screening con idrossiclorochina sulla pratica attuale. Am J Ophthalmol 2013;155:418..
5. Falcone PM, Paolini L, Lou PL. Idrossiclorochina tossicità nonostante la terapia a dose normale. Ann Ophthalmol 1993;25:385-388.
6. Browning DJ. Risposta alla definizione di peso corporeo ideale. Am J Ophthalmol 2002;134:935-936.
7. Blomquist PH, Chundru RK. Screening per la tossicità dell’idrossiclorochina da parte degli oftalmologi del Texas. J Rheumatol 2002;29:1665.
8. Wolfe F, Marmor MF. Tassi e predittori di idrossiclorochina tossicità retinica in pazienti con artrite reumatoide e lupus eritematoso sistemico. Arthritis Care Res 2010;62:775-784.
9. Cukras C, Huynh N, vitale S, Wong WT, Ferris III FL, setaccio PA. Test di screening soggettivo e oggettivo per la tossicità di idrossiclorochina. Ophthalmology 2015;122:356-366.
10. Lee MG, Kim SJ, Ham DI, Kang SW, Kee C, Lee J, Cha HS, Koh EM. Spessore delle cellule gangliari retiniche maculari – strato plessiforme interno in pazienti in terapia con idrossiclorochina. Invest Ophthalmol Vis Sci 2015;56:396-402.
11. FielderA, Graham E, Jones S, et al. Royal college of ophthalmologists linee guida: Tossicità oculare e idrossiclorochina. Eye 1998;12:907-909.
12. Marmor MF, Melles RB. Disparità tra campi visivi e tomografia a coerenza ottica nella retinopatia da idrossiclorochina. Ophthalmology 2014;121:1257-1262.
13. Mititelu M, Wong BJ, Brenner M, et al. Progressione degli effetti tossici di idrossiclorochina dopo la cessazione della terapia farmacologica. Nuove prove da imaging multimodale. Arch Ophthalmol 2013;131:1187-1197.
14. Wong KL, Pautler SE, Browning DJ. Maculopatia occhio di bue in riflettanza nel vicino infrarosso come un indicatore precoce di tossicità da idrossiclorochina. Clin Ophthalmol 2015; 9:521-5.
15. Petrie M, Durcan L. “The role of hydroxychloroquine blood levels in SLE” found at http://rheumnow.com/blog/role-hydroxychloroquine-blood-levels-sle#.VvaKbIfbwMQ.mailto. Accessed 28 September 2016.
16. Marmor MF, Kellner U, Lai TYY, Lyons JS, Mieler WF. Raccomandazioni rivedute sullo screening per la retinopatia da clorochina e idrossiclorochina. Ophthalmology 2011;118:415.
17. Browning DJ, Lee C. La sensibilità relativa e la specificità dei campi visivi 10-2, elettroretinografia multifocale e tomografia a coerenza ottica nel dominio spettrale nel rilevamento della retinopatia da idrossiclorochina e clorochina. Clinical Ophthalmology 2014;8:1389-1399.
18. Ding HJ, Denniston AK, Rao VK, Gordon C. Retinopatia legata all’idrossiclorochina. Rheumatology (Oxford) 2016;55:6:957-67.
0 commenti