Différence principale – Réactif vs Réactif
Une réaction chimique implique la réaction entre deux ou plusieurs composés pour fabriquer un ou plusieurs nouveaux composés. En d’autres termes, une réaction chimique est le changement des réactifs afin de former des produits. Ces réactifs peuvent être en phase solide, en phase liquide ou en phase gazeuse. Le terme réactif est utilisé pour décrire un type de réactifs. Les réactifs sont ajoutés à un mélange réactionnel pour la progression de la réaction. Cependant, contrairement aux réactifs, les réactifs ne sont pas nécessairement transformés en un autre composé. Ainsi, la principale différence entre réactif et réactif est que les réactifs sont consommés dans les réactions chimiques alors que les réactifs ne sont pas nécessairement consommés au cours de la progression d’une réaction.
Domaines clés couverts
1. Qu’est-ce qu’un réactif
– Définition, explication des propriétés avec exemples
2. Qu’est-ce qu’un réactif
– Définition, explication des propriétés avec exemples
3. Quelle est la différence entre réactif et réactif
– Comparaison des principales différences
Termes clés : Énergie d’activation, indicateur, produit, réactif, Réactif

Qu’est-ce qu’un réactif
Les réactifs sont la matière première qui subit des modifications au cours d’une réaction chimique. Les réactifs sont consommés lors d’une réaction chimique. Les liaisons chimiques des composés réactifs sont brisées afin de former de nouvelles liaisons, ce qui donne un nouveau composé. Ce nouveau composé est appelé le produit de la réaction.
Les molécules des réactifs peuvent être en phase solide, liquide ou gazeuse. Parfois, des réactifs qui sont dans des états physiques différents peuvent réagir entre eux pour former des produits. Une équation chimique montre les réactifs et le produit d’une réaction chimique. Une équation chimique utilise une flèche pour indiquer la direction de la réaction à partir de la tête de la flèche. Les réactifs se trouvent à gauche de la flèche tandis que les produits se trouvent à droite.
Lorsque l’on considère la cinétique des réactions chimiques, l’énergie potentielle des produits est déterminée par le type de réaction. Si la réaction est une réaction exothermique, alors les réactifs sont dans un niveau d’énergie élevé que celui des produits. Si la réaction est endothermique, alors les réactifs sont à un niveau d’énergie inférieur à celui des produits.
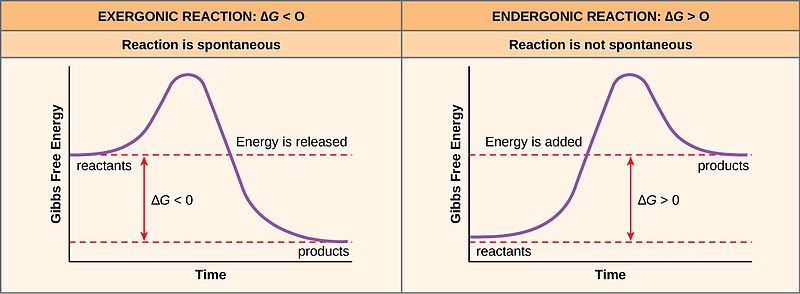
Figure 1 : Réactions exothermiques et endothermiques
Il existe cependant des éléments et des composés qui ne joueront jamais le rôle de réactifs en raison de leur absence de réactivité. On les appelle des composés inertes. Mais certains éléments et composés peuvent agir comme réactifs dans des conditions extrêmes. Par exemple, les gaz nobles ne deviennent pas des réactifs car ils sont totalement stables dans des conditions de température et de pression standard. Mais certains de ces gaz nobles peuvent devenir des réactifs dans des conditions extrêmes. Ex : le xénon (Xe) peut réagir avec le fluor gazeux.
Qu’est-ce qu’un réactif
Un réactif est un composé que l’on ajoute à un système afin de provoquer une réaction chimique. Ce réactif peut être consommé ou non lors de la réaction. S’il est consommé au cours de la réaction, alors ce réactif est appelé réactif. Mais parfois, les réactifs sont utilisés pour initier une réaction, pour obtenir une mesure de la réaction ou pour améliorer une réaction. Un réactif peut être en phase solide ou liquide avant d’être ajouté à un mélange réactionnel.
Par exemple, dans les réactions acide-base, on utilise des réactifs indicateurs pour déterminer le point final de la réaction. Ce réactif donne un changement de couleur au point final. Parfois, des réactifs catalyseurs sont utilisés pour améliorer une réaction chimique. Ces catalyseurs peuvent réduire l’énergie d’activation de la réaction.

Il existe des réactifs aux noms spécifiques qui sont utilisés à des fins spécifiques. Par exemple, le réactif de Grignard est utilisé dans la synthèse d’aldéhydes ou de cétones. Parfois, le réactif utilisé peut être récupéré après l’achèvement de la réaction. Mais, le réactif est parfois utilisé par la réaction comme réactif. Alors, il ne peut pas être récupéré pour une utilisation ultérieure.
Les réactifs reçoivent une évaluation lorsqu’ils sont produits. C’est ce que l’on appelle le « classement des réactifs ». Ce classement des réactifs indique la pureté du réactif et où utiliser ce réactif. Certains réactifs sont stockés dans des bouteilles sombres. En effet, ces réactifs sont sensibles à la lumière du soleil et peuvent être clivés en présence de lumière. Mais d’autres réactifs peuvent être stockés sans danger dans des bouteilles transparentes.
Différence entre réactif et réactif
Définition
Réactif : Les réactifs sont les matières premières qui subissent des modifications lors d’une réaction chimique.
Réactif : Les réactifs sont les composés qui sont ajoutés à un système afin de provoquer une réaction chimique.
Consommation
Réactif : Les réactifs sont essentiellement consommés dans les réactions chimiques.
Réactif : Les réactifs ne sont pas nécessairement consommés dans les réactions chimiques.
Application
Réactif : Les réactifs sont utilisés comme matière première d’une réaction chimique.
Réactif : Les réactifs sont utilisés pour mesurer, améliorer ou initier une réaction chimique.
Conclusion
Les termes réactif et réactif sont utilisés de manière interchangeable car les réactifs sont parfois consommés lors d’une réaction chimique. Mais, les réactifs peuvent souvent être distingués des réactants en fonction de leurs applications. Cependant, la principale différence entre réactif et réactif est que les réactifs sont consommés dans les réactions chimiques alors que les réactifs ne sont pas nécessairement consommés au cours de la progression d’une réaction.
1. « Réactifs et produits dans les réactions chimiques ». Les Nuls, Disponible ici. Consulté le 22 août 2017.
2. Helmenstine, Anne Marie. « Voici ce qu’est un réactif en chimie ». ThoughtCo, Disponible ici. Consulté le 22 août 2017.
Image courtoisie:
1. « Figure 06 03 03 » Par CNX OpenStax – (CC BY 4.0) via Commons Wikimedia
2. « Indicateur de pH coloré (cercle) » Par TheChimist – Travail propre (CC BY-SA 4.0) via Commons Wikimedia
![]()
.
0 commentaire